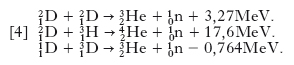neutrone
Particella elettricamente neutra, di dimensioni subatomiche (∿10–15 m) e massa di poco superiore a quella del protone (∿10–27 kg), appartenente alla famiglia degli adroni (➔ particelle elementari); insieme al protone, è uno dei costituenti del nucleo atomico, dal quale viene emesso in molte reazioni nucleari.
A sua volta il n., usato come proiettile per bombardare nuclei atomici, dà luogo a numerosissime reazioni nucleari, in molte delle quali vengono prodotti isotopi radioattivi, il cui studio approfondito ha permesso e permette di allargare le conoscenze sul nucleo. Il n., purché di energia sufficientemente bassa, costituisce così una sonda, unica e insostituibile, per l’esplorazione di certe proprietà della materia allo stato solido, liquido e gassoso. Esso inoltre è l’agente che inizia e mantiene le reazioni nucleari a catena che vengono utilizzate nei reattori nucleari, destinati alla ricerca o alla produzione di energia su scala industriale (➔ reattore), e nelle armi nucleari, per es. la bomba a n. (➔ nucleare).
Per quanto concerne le interazioni forti, il n. e il protone costituiscono i due diversi stati di carica della medesima particella: il nucleone.
La scoperta del neutrone
La scoperta del n. ebbe origine da alcune classiche esperienze di W. Bothe e H. Becker, i quali a Berlino-Charlottenburg nel 1930 osservarono una radiazione secondaria penetrante emessa da vari elementi leggeri (Li, Be, B, F ecc.) bombardati con particelle alfa emesse da un campione di polonio, e la interpretarono come costituita da raggi gamma duri, ossia molto penetranti. Poco dopo, J. Chadwick, a Cambridge (Gran Bretagna), dimostrò sperimentalmente che la radiazione penetrante in questione era capace di trasferire energie dello stesso ordine di grandezza anche a nuclei di azoto, i quali sono dotati di una massa circa 14 volte quella del protone. Chadwick si rese subito conto che tutti i fenomeni fino ad allora osservati potevano essere pienamente spiegati se si faceva l’ipotesi che la radiazione penetrante fosse costituita, almeno in parte, da un nuovo tipo di corpuscoli elettricamente neutri e dotati di una massa molto prossima a quella del protone. I risultati delle sue esperienze e questa loro interpretazione furono pubblicati da Chadwick in una lettera al giornale scientifico inglese Nature il 17 febbraio 1932, lettera che universalmente è considerata come l’atto di nascita del neutrone.
Da queste prime esperienze e da altre eseguite poco dopo, fu possibile stabilire che la massa del nuovo corpuscolo, il n., era di assai poco superiore a quella del protone (v. tab.). Il fatto poi che i n. fossero emessi da nuclei di elementi leggeri sotto l’azione di particelle alfa, suggeriva un nuovo modello di nucleo. Prima della scoperta del n. si pensava infatti che i nuclei di tutti gli atomi consistessero in aggregati dei due corpuscoli elementari allora noti, protoni ed elettroni, in quantità tali da dar luogo, nel loro insieme, a un sistema dotato del giusto valore della carica elettrica e della massa. Ma con l’avvento della meccanica quantistica, di pochi anni precedente, questo modello era diventato inaccettabile: come conseguenza del principio di indeterminazione, un elettrone confinato entro le dimensioni di un nucleo (∿10–14 m) era necessariamente dotato di una quantità di moto, e quindi anche di un’energia cinetica, così elevata da essere incompatibile con quanto si sapeva già allora sulle energie in gioco nei nuclei. La scoperta del n. apriva una via d’uscita a questa difficoltà. Diventava infatti possibile l’ipotesi che non vi fossero elettroni nel nucleo, e che questo fosse costituito solo di protoni e di neutroni. Infatti, la difficoltà sopra accennata nel caso degli elettroni non esiste nel caso di protoni e n.; a causa della loro massa, che è circa 2000 volte maggiore di quella degli elettroni, il limite inferiore che si deduce dal principio di indeterminazione per la loro energia cinetica è pienamente compatibile con le energie in gioco nei nuclei. Nasceva così un nuovo modello di nucleo costituito solo da protoni e n. (F. Perrin, W. Heisenberg, D. Ivanenko, 1932), ampiamente confermato da tutte le esperienze successive. In questo modello ogni nuclide è individuato da due numeri, il numero Z di protoni e il numero N di n. che lo costituiscono; la sua carica elettrica è pari a Ze, essendo e il valore assoluto della carica dell’elettrone, e la sua massa (in unità di massa atomica) è sempre molto pros;sima al cosiddetto numero di massa A=Z+N. Spesso per individuare un nuclide, invece di dare i due numeri interi Z e N, si danno i numeri interi A e Z. Così, per es., quando si scrive 2713Al s’intende un nuclide composto di Z=13 protoni e N=A−Z=27−13=14 neutroni. Il numero Z, in questo caso 13, viene chiamato numero atomico in quanto esso fissa l’elemento chimico cui appartiene il nuclide considerato, in questo caso l’alluminio. In questa notazione, il n. è indicato con il simbolo l0n e il protone con l’uno o l’altro dei due simboli l1p oppure l1H.
Due scoperte compiute da E. Fermi e collaboratori, strettamente legate fra loro, dettero un impulso straordinario allo studio delle reazioni nucleari e delle proprietà dei neutroni. Nel gennaio 1934, I. Curie e F. Joliot avevano scoperto che alcuni elementi leggeri, in particolare il boro e l’alluminio, bombardati con particelle alfa, davano origine a sostanze radioattive (radioattività artificiale per bombardamento di particelle alfa). Immediatamente dopo la divulgazione di questi risultati, Fermi a Roma pensò di provocare la radioattività artificiale usando come proiettili i n., nonostante questi, essendo corpuscoli prodotti in reazioni nucleari iniziate da particelle alfa, fossero allora disponibili solo con intensità molto piccole, dell’ordine di 104-105 volte minori delle intensità delle sorgenti di particelle alfa usate dai coniugi Joliot-Curie. Fermi partiva dall’idea che la mancanza di carica elettrica del n., grazie alla quale esso non è respinto da un nucleo quando passa nelle sue vicinanze, potesse più che compensare il loro basso numero. La scoperta della radioattività artificiale per bombardamento di n., fatta da Fermi nel marzo 1934, risultò particolarmente interessante anche per la varietà e l’importanza dei fenomeni scoperti nello studio sistematico, eseguito in vari centri di ricerca e in particolare a Roma da Fermi e collaboratori (E. Amaldi, O. D’Agostino, F. Rasetti, E. Segré). Già nel corso del 1934 fu dimostrato che i n. possono produrre processi di diverso tipo, indicati con i simboli (n, α), (n, p) e (n, γ), dove la prima e la seconda lettera fra parentesi rappresentano rispettivamente la particella incidente e la particella emessa. Fu anche dimostrato, a Roma, che l’ultimo dei suddetti processi, indicato spesso con il nome di cattura radiativa del n., può essere prodotto in tutti gli elementi chimici, dai più leggeri fino ai più pesanti, come il torio e l’uranio.
Negli anni successivi, in diversi laboratori furono scoperti molti altri tipi di reazioni nucleari provocate da n., come, per es., i processi (n, 2n), (n, 3n) ecc. Particolarmente importante fu la scoperta fatta, nel 1939 a Berlino, da O. Hahn e F. Strassmann, i quali dimostrarono che, sotto l’azione dei n., elementi pesanti, come il torio e l’uranio, subiscono il fenomeno della fissione.
I n. lenti
Nell’ottobre del 1934, sulla base dei risultati di un’esperienza eseguita con i suoi collaboratori (ai quali si era unito B. Pontecorvo), Fermi formulò le ipotesi che: a) nelle sostanze idrogenate (per es., nell’acqua, o nella paraffina) l’energia dei n. può essere enormemente ridotta in seguito a un numero grande, ma non grandissimo, di urti elastici successivi contro i protoni; b) i n. così rallentati, indicati fin da allora come n. lenti, sono molto più efficaci dei n. veloci nel produrre certe reazioni nucleari, in particolare le reazioni (n, γ). Queste due ipotesi furono confermate pienamente a mezzo di numerose esperienze eseguite dal gruppo di Roma, come anche da altri gruppi, tanto che in breve tempo furono considerate non come ipotesi, ma come fatti ben accertati. Fu anche dimostrato, fin dall’autunno 1934, che la proprietà a) non è esclusiva delle sostanze idrogenate, ma comune a tutte le sostanze contenenti un’alta percentuale di elementi leggeri purché poco assorbenti dei neutroni. Inoltre, esperienze eseguite in vari laboratori nel corso del 1935 permisero di stabilire che nel processo di rallentamento l’energia dei n. viene degradata fino a raggiungere l’energia di agitazione termica delle molecole; da questo momento in poi i n. non possono più seguitare a perdere energia ma si muovono, attraverso il materiale usato per il loro rallentamento, con l’energia di agitazione termica; il loro moto è simile a quello delle molecole di un gas rarefatto che diffonda entro un materiale spugnoso. Questo processo, prima di rallentamento e poi di diffusione termica, viene sempre interrotto o perché il n. sfugge dalla superficie del materiale rallentante o perché esso viene catturato da uno dei nuclei presenti. Alcuni anni dopo fu introdotto il termine moderatore per indicare qualunque materiale che si presti a provocare il rallentamento dei n. e a mantenere successivamente, per un tempo abbastanza lungo, il processo di diffusione termica.
Per molti problemi, la grandezza che caratterizza il comportamento del n., più che la sua energia cinetica o la sua velocità, è la sua lunghezza d’onda di de Broglie λ, legata alla quantità di moto p dalla relazione λ=h/p, dove h è la costante di Planck. Per n. di energia non molto elevata (la cui velocità sia molto minore di quella della luce nel vuoto) si ha
[1] formula
E essendo misurata in eV. Questa formula mette bene in evidenza le straordinarie possibilità che sono aperte allo sperimentatore che lavora con n.: per energie di 100 MeV la lunghezza d’onda è dell’ordine di grandezza delle dimensioni delle particelle elementari; a 1 MeV è dell’ordine delle dimensioni di un nucleo; a 10−3-10−4 eV è dell’ordine delle dimensioni atomiche. Raffreddando il moderatore a temperature molto basse, e facendo uso di opportuni monocromatori e selettori di velocità, si possono avere n. la cui lunghezza d’onda è di migliaia di ångström.
Le principali proprietà del neutrone
Le principali proprietà del n. in quiete sono raccolte in tab. insieme a quelle del protone, che servono di confronto. Le masse di questi due corpuscoli sono date nella prima colonna, in unità di massa atomica, in kg e in MeV/c2. Come si vede, la differenza tra le due masse (ca. 1,29 MeV/c2) è molto piccola, in accordo qualitativo con le prime stime approssimative fatte da Chadwick. Nella seconda colonna è data la carica elettrica Q in termini della carica elettronica e, e nella terza lo spin o momento della quantità di moto intrinseco J, espresso in unità di ℏ. Il n., avendo spin semintero come il protone e l’elettrone, ubbidisce al principio di Pauli e quindi alla statistica di Fermi, cioè è un fermione. Nella quarta colonna sono i momenti magnetici, μ, espressi in magnetoni nucleari, μN (pari a 1/1836 del magnetone di Bohr). Essi sono considerati come anomali, nel senso che i loro valori differiscono da quelli prevedibili sulla base della teoria sviluppata da P.A.M. Dirac all’inizio degli anni 1930, che descrive il comportamento degli elettroni in modo soddisfacente; se si applica l’equazione di Dirac al protone e al n., si trova che il primo deve avere un momento magnetico pari a 1 magnetone nucleare e che il secondo deve avere momento magnetico nullo, avendo carica elettrica nulla. Il fatto che il protone e il n. siano dotati di momento magnetico anomalo costituisce una chiara indicazione di una struttura complessa di questi due corpuscoli. Nella quinta colonna è infine data la vita media, τ. Come si nota, il n. è instabile; il n. libero decade secondo il processo
[2] formula
ossia si trasforma spontaneamente in un protone emettendo un elettrone (e−) e un antineutrino (ν̄e).
Si è parlato di n. liberi, in quanto il comportamento dei n. legati in un nucleo è determinato dall’essere soddisfatte o no certe condizioni di stabilità riguardanti il nucleo nel suo insieme. Nei nuclei stabili il precedente processo di decadimento è reso impossibile da condizioni energetiche, che invece non sono soddisfatte nei nuclei radioattivi per emissione di elettroni: in questi, uno dei n. presenti subisce tale processo con una vita media determinata dalla struttura del nucleo particolare considerato. Il n. libero è dunque una particella (debolmente) instabile che decade con una vita media di circa 15 minuti, a differenza del protone, per il quale è stato stabilito un limite inferiore della vita media di 1032 anni.
Lo studio sperimentale delle interazioni fra il n. ed elettroni di alta energia ha evidenziato che il n., pur globalmente neutro, possiede una struttura elettromagnetica; il valore del raggio quadratico medio della distribuzione di carica elettrica nel n. è risultato essere 0,33 ∙ 10–15 m, cioè dello stesso ordine di grandezza di quello del protone. Lo studio della diffusione anelastica profonda di elettroni di altissima energia su n. ha ulteriormente precisato questa struttura interna: un n. è costituito da due quark down e da un quark up (➔ quark).
Interazioni del n. con altre particelle
Il n. (al pari del protone) dà luogo a tutte le interazioni oggi note: interazioni gravitazionali, interazioni deboli, interazioni elettromagnetiche e interazioni forti. Che il n. sia soggetto alla gravitazione è stato dimostrato da vari ricercatori misurando la curvatura della traiettoria parabolica descritta da n. di bassissima energia sotto l’azione del campo gravitazionale terrestre. Il n. subisce anche interazioni deboli, come è dimostrato dal processo di decadimento caratteristico di questa interazione. Oggi si conoscono vari altri tipi di processi dovuti alle interazioni deboli, ma il processo di decadimento beta del n. fu il primo a essere scoperto. Esso fu introdotto da E. Fermi nel 1933 come punto di partenza della sua teoria della disintegrazione beta dei nuclei, la quale, ampliata e approfondita grazie a un notevole lavoro sperimentale e teorico, soprattutto a partire dal 1958, conserva ancora la sua validità essenziale.
Le interazioni elettromagnetiche sono in generale enormemente più intense delle interazioni deboli: l’origine di questa interazione nel caso del n. è dovuta al fatto che il n., pur essendo la sua carica elettrica totale nulla, possiede una distribuzione interna di carica.
Restano infine le interazioni forti, le quali sono, grosso modo, mille volte più intense delle interazioni elettromagnetiche. Nel caso dei n. e protoni di energia non troppo elevata esse vengono indicate con il nome di forze nucleari in quanto sono queste interazioni che, agendo fra le varie particelle costituenti il nucleo, determinano la sua energia di legame e i suoi livelli energetici eccitati, e le distribuzioni spaziali dei protoni e dei n. che lo compongono (➔ forza).
Sorgenti di neutroni
Le sorgenti usate nelle prime ricerche che portarono alla scoperta del n. e ai primi studi delle sue proprietà erano tutte basate sulle reazioni (α, n) prodotte in elementi leggeri. Nel caso del berillio, l’elemento che fornisce un’intensità particolarmente alta, la reazione è
[3] formula
Come corpi emettitori alfa si usavano allora, e anche in seguito, a seconda dei casi: 210Po, 226Ra, 222Rn, ai quali si sono aggiunti più tardi 239Pu, 241Am e 242Cm. Sorgenti di questo tipo, contenenti sostanze radioattive alfa a lunga vita media (per es., 226Ra, con periodo di dimezzamento di 1600 anni) sono rimaste in uso come sorgenti standard; una sorgente contenente Ra+Be emette, tutt’intorno, circa 1,4∙107 n. al secondo per grammo di Ra. Quando si disponga di un acceleratore che permetta di accelerare protoni, deutoni o tritoni a energie dell’ordine di almeno qualche MeV, si preferiscono altre reazioni; alcune di queste sono le seguenti
[4] formula
La scelta dell’una o dell’altra di queste reazioni dipende dall’acceleratore di particelle di cui si dispone e dallo spettro di n. (veloci) che si desidera produrre.
Per produrre n. di energia superiore a circa 50 MeV si fa ricorso a due altri tipi di processi: le reazioni di strappo (stripping) del deutone e l’urto con scambio di carica di un protone contro un n. di un nucleo. Nelle reazioni di strappo un deutone incidente, passando vicino a un nucleo, si strappa: il suo protone resta, per così dire, catturato nel nucleo, che subisce successivamente uno o più processi di disintegrazione, mentre il suo n. prosegue, in una direzione prossima a quella del deutone incidente, con circa la metà dell’energia cinetica che questo possedeva inizialmente. I processi di scambio di carica vengono usati a grandissime energie (dell’ordine del GeV e oltre) e consistono nel fatto che, a queste energie, un protone nell’attraversare un nucleo dà luogo abbastanza frequentemente a un urto con uno dei n. circostanti, molto simile a un urto elastico, salvo che le due particelle si scambiano le loro cariche elettriche. Questo processo viene facilmente interpretato nel quadro delle concezioni secondo cui il protone e il n. sono due stati diversi di una stessa particella, il nucleone: lo scambio di carica è dovuto al trasferimento di un mesone positivo dal protone incidente al n. urtato. La particella che rincula diventa un protone, mentre un n. prosegue con una quantità di moto non molto diversa, in direzione e modulo, da quella che competeva al protone incidente.
Per produrre n. lenti ci si può servire di una qualunque delle sorgenti sopra descritte, contornate da un moderatore. Le sorgenti di gran lunga più intense di n. lenti sono tuttavia costituite dai reattori nucleari (➔ reattore). Tali sorgenti sono sempre più spesso sostituite da sorgenti a spallazione (➔) che forniscono fasci neutronici di altissima qualità con intensità largamente superiori.
Impieghi e diffrazione dei neutroni
I n. hanno trovato numerose importanti applicazioni in campi di tipo così diverso da rendere ardua una loro elencazione. Occupano il primo posto, per gli aspetti industriali ed economici, i reattori nucleari. Si sono anche costruiti reattori nucleari dotati di caratteristiche speciali, che li rendono particolarmente adatti per produrre flussi di n. di elevata intensità nella loro regione centrale: tali flussi neutronici possono essere utilizzati in loco per produrre considerevoli quantitativi di sostanze radioattive artificiali, oppure, attraverso opportuni canali, possono essere portati all’esterno del reattore, anche a distanze notevoli, in modo da poterli utilizzare nel modo migliore per eseguire ricerche di interesse scientifico e tecnologico. In questo contesto l’espressione ‘interesse scientifico’ non si riferisce soltanto a ricerche riguardanti le proprietà dei n. o la struttura nucleare, ma a ricerche riguardanti altri campi della fisica, come la fisica dei solidi o, più in generale, degli stati aggregati, o addirittura lo studio di certi processi chimici e biologici.
Fra i molteplici impieghi dei radioisotopi, la tecnica dei traccianti ha reso possibili molti fra i più importanti progressi fatti dalla farmacologia e dalla biologia moderne a partire dagli anni 1950.
Un’applicazione dei n. degna di menzione è lo studio delle strutture molecolari di sostanze liquide e gassose, e soprattutto di sostanze cristalline, a mezzo dei fenomeni di diffrazione cui i n. danno luogo. Essa è qualitativamente simile alla diffrazione dei raggi X, nel senso che, se l’una o l’altra di queste radiazioni incide sulla superficie di un cristallo in una direzione che forma un angolo ϑ con i piani reticolari, si osserva un massimo dell’intensità della radiazione riflessa quando è soddisfatta la condizione di Bragg mλ=2dsen ϑ, dove λ è la lunghezza d’onda della radiazione, m è un numero intero positivo (detto ordine di riflessione) e d la distanza fra i piani reticolari in oggetto. Poiché d è dell’ordine di qualche ångström, per poter osservare questo fenomeno per valori di ϑ non troppo piccoli, è necessario che anche λ sia dello stesso ordine di grandezza. Come si vede dalla [1], questa condizione è soddisfatta, per es., da n. di energia dell’ordine di kT a temperatura ambiente, cioè dell’ordine di 0,025 eV, per i quali si ha λ=1,81 Å. La diffrazione dei n. lenti differisce, tuttavia, da quella dei raggi X o degli elettroni perché questi interagiscono elettromagneticamente anche con gli elettroni atomici mentre i n. subiscono la diffusione solo da parte del nucleo atomico; questo ha dimensioni piccolissime rispetto alla lunghezza d’onda dei n. e pertanto non si hanno i fenomeni di interferenza, e la diffusione subita dai n. da parte di un singolo atomo è isotropa, ossia indipendente dall’angolo di diffusione.
Quando la radiazione neutronica è diffusa da un insieme di atomi disposti regolarmente (come si verifica in una molecola o, in modo ancor più evidente, in un cristallo) e si osservano i fenomeni di interferenza cui essi danno luogo, si nota che solo una parte delle onde diffuse sono coerenti e concorrono quindi all’interferenza; la parte incoerente è dovuta alle vibrazioni termiche degli atomi attorno a posizioni di equilibrio, alla presenza di diversi isotopi di uno stesso elemento chimico distribuiti a caso (e che diffondono i n. in modo diverso l’uno dall’altro) e all’orientamento disordinato degli spin nucleari rispetto agli spin dei n. incidenti. A seconda del nuclide considerato, la parte coerente della radiazione neutronica viene diffusa senza cambiamento di fase o con cambiamento di fase di 180° rispetto all’onda neutronica incidente. Anche sotto questo aspetto, dunque, i n. mostrano un comportamento diverso da quello dei raggi X, per i quali non si ha sfasamento fra onda incidente e onda sparpagliata. Da queste brevi osservazioni è chiaro che la diffrazione dei n. può fornire, in generale, informazioni diverse da quelle che si deducono dalla diffrazione dei raggi X o degli elettroni da parte dello stesso cristallo. A differenza di questa (per la quale le sezioni d’urto crescono con il numero atomico), essa permette, per es., di localizzare gli atomi di idrogeno disposti in un cristallo fra atomi di elevato numero atomico, oppure di distinguere nuclidi dotati di numeri atomici molto vicini nella stessa matrice cristallografica, o di raffinare la conoscenza delle strutture di liquidi o solidi amorfi, e così via.
Neutronigrafia
La neutronigrafia è una tecnica usata per ricavare immagini della struttura di oggetti vari, opachi alla luce ordinaria, attraversati da un fascio di n. di conveniente energia. Il termine è usato anche per indicare l’immagine ottenuta con tale tecnica.
Per la neutronigrafia si ricorre di solito a n. lenti, forniti da un reattore nucleare di ricerca o da altra idonea sorgente. I n., dopo avere attraversato l’oggetto in esame, colpiscono un convertitore, il quale può essere di due tipi: indiretto o diretto. Un convertitore indiretto è costituito da una lamina d’oro o d’iridio o di disprosio, molto sottile, in cui i n. lenti producono, attraverso un processo (n, λ), isotopi radioattivi. La radioattività indotta in ogni punto del convertitore è proporzionale all’intensità trasmessa del fascio neutronico, cosicché, dopo un’esposizione di opportuna durata, si ha una vera e propria immagine radioattiva. Tale immagine viene quindi trasferita, lontano dal fascio di n., a una pellicola fotografica particolarmente sensibile ai raggi beta, con cui il convertitore viene mantenuto in contatto per un tempo opportuno o ricostruita mediante una camera proporzionale a molti fili. In tal modo, la presenza di raggi gamma, che spesso accompagnano i n., non dà luogo ad alcun inconveniente.
Se il fascio neutronico è privo di raggi gamma, può convenire l’uso di un convertitore diretto, costituito da uno scintillatore per n. che, durante l’esposizione al fascio di n., è mantenuto a contatto con la pellicola fotografica. La neutronigrafia non è equivalente alle ordinarie radiografie con raggi X o gamma in quanto queste radiazioni, una volta fissata la loro energia, hanno un coefficiente di assorbimento che è una funzione crescente e regolare del numero atomico Z del materiale su cui incidono. Il coefficiente di assorbimento di n., invece, non è legato in modo semplice né al numero atomico né al numero di massa dei diversi nuclidi, e varia al variare dell’energia in modo irregolare e molto diverso non solo da elemento a elemento, ma anche da isotopo a isotopo di uno stesso elemento. Pertanto, scegliendo opportunamente l’energia dei n. o ripetendo la neutronigrafia successivamente con n. di diversa energia, è possibile analizzare la struttura di un oggetto ricavando informazioni complementari a quelle ottenute mediante radiografie ordinarie.