PET
Sigla di positron emission tomography, metodica della medicina nucleare che permette di ottenere immagini di distribuzione tridimensionale della radioattività all’interno di una sezione corporea, recuperando così l’informazione in profondità, non ottenibile con la scintigrafia. Con la tomografia computerizzata a emissione di fotoni singoli, o SPECT (single photon emission computed tomography), ha trovato largo impiego nella clinica, specialmente in neurologia, consentendo una fine analisi a livello dell’attività metabolica del sistema nervoso centrale, e quindi la diagnosi precoce di molte importanti affezioni, come la demenza di Alzheimer o il morbo di Parkinson.
Funzionamento
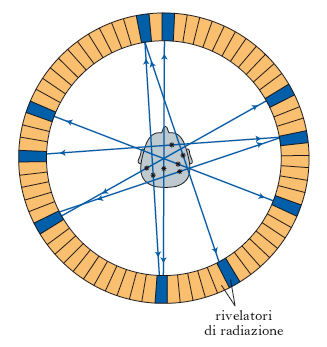
La PET impiega isotopi radioattivi emittenti positroni (β+, cioè particelle aventi la stessa massa e carica di un elettrone, ma segno opposto, positivo), prodotti mediante un ciclotrone (v. fig.). Un positrone emesso durante il decadimento radioattivo si propaga nel mezzo circostante (nel caso dei tessuti umani, per pochi millimetri), perdendo parte dell’energia cinetica in interazioni successive. Quando l’energia cinetica della particella si è ridotta a livelli confrontabili con quella di agitazione termica dell’ambiente, il positrone interagisce con un elettrone della materia in un processo detto di annichilazione. In tale processo, le due particelle scompaiono e le masse delle due particelle si convertono in energia, generando due radiazioni gamma. La rivelazione di questi due fotoni da parte di una coppia di rivelatori posti in coincidenza temporale permette di identificare la linea che congiunge i centri dei due rivelatori come quella lungo la quale è avvenuto il processo di annichilazione, e costituisce la base di un sistema PET. Durante uno studio PET, il paziente si trova all’interno del sistema di rivelazione in posizione supina. I dati registrati dalle singole coppie di rivelatori vengono inizialmente trasferiti e memorizzati su supporti magnetici, per essere poi rielaborati al fine di ricostruire la distribuzione del tracciante radioattivo nelle sezioni corporee in esame. Il potere di risoluzione della PET è pari a circa 5-9 mm.
PET cerebrale
La PET permette di indagare aspetti funzionali biochimici e metabolici dell’encefalo. Il principio su cui si basa è legato alla possibilità di marcare composti di interesse biologico, come il glucosio, l’H2O o i neurotrasmettitori, con isotopi radioattivi che, non modificando la struttura e il comportamento biochimico, permettono di seguirne il destino all’interno del tessuto cerebrale.
Applicazioni cliniche. - È stato dimostrato che esiste una corrispondenza tra la captazione di 18F-FDG (fluoro-desossiglucosio) e il grado istologico di malignità dei tumori cerebrali. La PET consente di distinguere, in pazienti già sottoposti a intervento neurochirurgico o a radioterapia per tumore cerebrale, un danno tessutale aspecifico (edema, necrosi), dovuto al trattamento, da una recidiva tumorale.
Un elevato numero (20%) di pazienti con epilessia non può essere controllato per mezzo della terapia farmacologica. In questi soggetti, qualora la sede e l’estensione della zona epilettogena lo consentano, può essere preso in considerazione il trattamento chirurgico di ablazione del focolaio epilettogeno. Poiché nella maggioranza dei casi con la tomografia computerizzata (TC) e la risonanza magnetica (RM) non sono riscontrabili anomalie strutturali, per valutare l’estensione dei focolai epilettogeni sono state sviluppate e applicate particolari tecniche di localizzazione, quali l’elettroencefalografia intraoperatoria e la registrazione effettuata da elettrodi impiantati in profondità con metodo stereotassico. A queste tecniche invasive e complesse si sono affiancati gli studi PET con 18F-FDG. Eseguiti durante il periodo interictale, essi hanno mostrato una riduzione di metabolismo nelle aree cerebrali interessate, in accordo con i dati provenienti dalle indagini elettrofisiologiche.
La PET nella ricerca clinica. - Al di là degli impieghi clinici, la PET rappresenta, per la sua versatilità e molteplicità di applicazioni, uno strumento unico per studi di fisiopatologia in vivo. La possibilità di studiare aspetti funzionali quali il flusso ematico cerebrale (rCBF) con C15O2, il consumo (CMRO2) e l’estrazione (OER) di ossigeno con 15O2, il metabolismo glucidico (CMR glu) con 18F-FDG e, più di recente, il sistema dei neurotrasmettitori cerebrali (marcando i neurotrasmettitori con 11C o 18F), ha consentito notevoli progressi nel campo delle neuroscienze. In particolare, in ambito di patologia cerebrovascolare la misurazione con tecnica PET di diversi parametri permette di eseguire il monitoraggio in vivo dei fenomeni che dall’ischemia ancora reversibile portano all’infarto cerebrale con necrosi tessutale. Nella patologia degenerativa, gli studi PET del metabolismo cerebrale con 18F-FDG hanno permesso di individuare schemi dell’attività metabolica correlabili al tipo e alla gravità della malattia. Nella demenza di Alzheimer, la depressione metabolica coinvolge in modo specifico le aree temporali e parietali bilateralmente, con una distribuzione corrispondente a quelle che sono le maggiori alterazioni topografiche anatomopatologiche. Nella malattia di Parkinson, oltre a una depressione metabolica a carico dei gangli della base, si sono evidenziate riduzioni del metabolismo corticale correlabili alla presenza di depressione o di deficit cognitivi. La PET con impiego di fluorodopa marcata con 18F è utilizzata per lo studio della funzione dopaminergica in vivo. Di particolare rilevanza è stata la dimostrazione delle alterazioni nella produzione e nel metabolismo della dopamina nella malattia di Parkinson, in cui la lesione principale riguarda il sistema dopaminergico presinaptico nigro-striatale. Con l’impiego di traccianti a breve emivita è anche possibile studiare il fenomeno dell’attivazione di specifiche aree cerebrali durante l’esecuzione di precisi compiti cognitivi. Si identifica così l’anatomia funzionale dei processi di linguaggio, attenzione e programmazione del movimento. Ciò consente di acquisire nuove conoscenze in ordine alle modalità operative con cui il cervello processa ed elabora il pensiero.
PET cardiaca
Lo studio del metabolismo del miocardio rappresenta un altro dei campi di applicazione clinica della PET. Il glucosio e gli acidi grassi liberi rappresentano i principali substrati energetici del miocardio e il loro metabolismo può essere valutato in vivo con traccianti emittenti positroni. Il 2-fluoro-2-desossiglucosio marcato con 18F(18F-FDG) è il tracciante in uso per gli studi PET del metabolismo glucidico. Il tracciante viene somministrato per via endovenosa alla dose di 3,7 MBq/kg di peso corporeo e le immagini tomografiche sono acquisite dopo circa 40 minuti, onde permettere una buona concentrazione intracardiaca di glucosio-6-fosfato. Nel soggetto normale, l’accumulo di 18F-FDG è minimo; infatti, per produrre energia il cuore utilizza il processo di beta-ossidazione degli acidi grassi. L’ischemia provoca invece importanti alterazioni dell’utilizzazione degli acidi grassi da parte del tessuto miocardico. Nel miocardio ischemico, un’aumentata captazione di FDG riflette un aumento della glicolisi anaerobica ed è indicativa della presenza di vitalità tessutale. L’assenza di captazione del 18F-FDG è apprezzabile sia nel miocardio necrotico sia in quello normoperfuso. Tale osservazione è di notevole importanza per un corretto inquadramento clinico; si è infatti osservato in studi eseguiti con doppio tracciante, sia per la perfusione (201Tl, 99mTc-MIBI) sia per la vitalità miocardica (18F-FDG), che il 50% delle aree, che negli studi perfusionali apparivano necrotiche, risultava vitale per l’accumulo elettivo di 18F-FDG. Un simile approccio si dimostra utile nel contesto clinico, in particolare quando vi sia indicazione a interventi terapeutici di rivascolarizzazione miocardica.