sclerosi laterale amiotrofica
sclerosi laterale amiotrofica
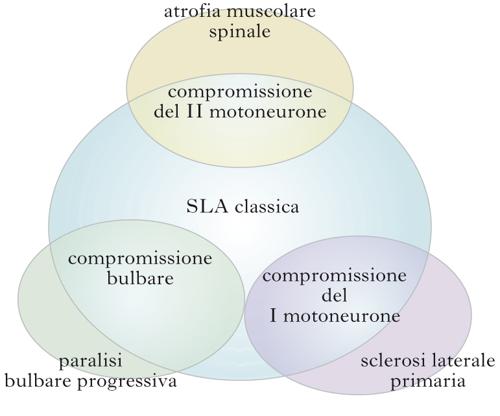
Patologia neurodegenerativa (in sigla SLA) caratterizzata da progressiva paralisi muscolare, che riflette la degenerazione dei motoneuroni (➔) a livello della corteccia cerebrale, del tronco encefalico e del midollo spinale. Il termine amiotrofico sta a indicare l’atrofia delle fibre muscolari; sclerosi si riferisce alla sostituzione in tessuto gliotico (➔ gliosi) a cui va incontro il tessuto nervoso; laterale si riferisce, invece, al coinvolgimento del tratto corticospinale anteriore e laterale. La SLA rappresenta la forma più comune di malattia del motoneurone, ossia di un insieme di patologie caratterizzate dalla compromissione primaria dei neuroni di moto centrali o periferici; a essa appartengono, oltre alla SLA, anche la sclerosi laterale primaria (➔), l’atrofia muscolare spinale (SMA), la paralisi bulbare progressiva. In Italia ha una prevalenza di 7,89/100.000 e un’incidenza di 2,96/100.000 abitanti nella popolazione. L’età media di insorgenza è di 55÷65 anni e solo il 5% ha un esordio prima dei 30 anni. Sono colpiti prevalentemente gli uomini, con un rapporto M/F pari a 1,5:1. La sopravvivenza media è di 36 mesi. La paralisi è progressiva e conduce a morte per insufficienza respiratoria entro 2÷3 anni in caso di esordio bulbare e 3÷5 anni a seguito di esordio spinale.
Patogenesi
La SLA è una patologia sporadica nella quasi totalità dei casi; le forme familiari variano dal 5 al 10% dei casi e si trasmettono come carattere autosomico dominante con penetranza età-dipendente. Per SLA familiare (FALS) si intende una SLA diagnosticata in almeno 2 individui consanguinei separati da non più di 4 generazioni. Fino a ora sono stati individuati vari geni responsabili della FALS, tra questi quelli di maggiore rilevanza sono Sod 1, Alsyna, Fus/Tls, Tardbp. Le mutazioni riscontrate nelle forme sporadiche (SALS) riguardano mutazioni de novo, ossia sviluppate in un secondo momento e non ereditate con il patrimonio genetico dei genitori. Alla luce di recenti studi vanno ricercate mutazioni anche a livello del DNA mitocondriale. Il fenotipo di manifestazione della patologia può essere spinale (vale a dire con compromissioni della forza muscolare e della motilità a livello degli arti superiori o inferiori) e bulbare (per interessamento dei motoneuroni dei nervi cranici, con comparsa di disfagia, disartria, disturbi della deglutizione, della respirazione e della fonazione). La forma spinale si presenta nei 2/3 dei pazienti, mentre la forma bulbare è più frequente nelle donne. La patogenesi della SLA non è perfettamente nota: può essere considerata una patologia multifattoriale, nella quale concorrono vari fattori tra cui i fattori genetici, il danno eccitotossico (per l’azione sui recettori del glutammato), lo stress ossidativo (eccesso di radicali liberi dell’ossigeno che inducono morte cellulare) e le disfunzioni mitocondriali (accumulo di calcio e ridotta attività della catena respiratoria cellulare, con deficit del metabolismo energetico).
Segni e sintomi
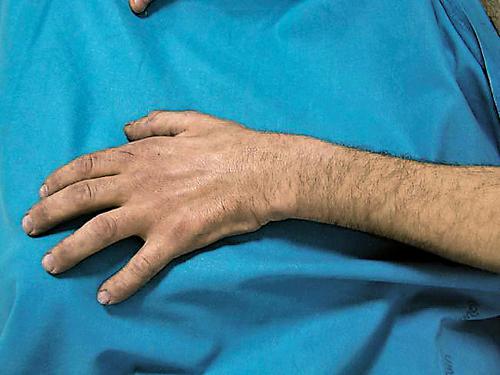
Il quadro clinico più comune di presentazione della SLA è caratterizzato da segni di lesione centrale spinale agli arti inferiori (spasticità, aumento dei riflessi osteotendinei e riflesso cutaneo plantare in estensione (o segno di Babinski) e segni di compromissione periferica agli arti superiori (deficit di forza, atrofia muscolare prevalentemente ai muscoli delle mani, dette mani ‘ad artiglio’. In genere il soggetto non presenta disturbi delle sensibilità (anche se in tempi recenti sono stati descritti casi di interessamento del sistema sensitivo nel 10÷20% dei pazienti) e il controllo sfinterico è solitamente conservato, anche quando è presente un importante deficit di forza (per preservazione del nucleo di Onuf, ossia del nucleo localizzato a livello del midollo spinale, che innerva i muscoli striati del pavimento pelvico).
Diagnosi
La diagnosi viene effettuata mediante la valutazione della storia clinica, un esame obiettivo neurologico e l’esame elettromiografico (EMG), volto a riscontrare segni precoci di danno neurogeno, anche nei distretti corporei clinicamente non colpiti. L’esame EMG mostra potenziali di unità motoria polifasici, con aumento in ampiezza e durata, mentre il muscolo a riposo presenta potenziali di fibrillazione e fascicolazione. Le fascicolazioni sono spesso percepite dal paziente come ‘guizzi sotto la pelle’. La diagnosi differenziale si pone con varie patologie che possono mimare il quadro clinico della SLA, tra le quali la mielopatia cervicale di origine artrosica, la neuropatia motoria multifocale e la malattia di Kennedy. La SLA viene suddivisa in: clinicamente definita, clinicamente probabile, clinicamente probabile con supporto di laboratorio e clinicamente possibile. Per porre diagnosi di SLA è comunque necessario che i segni e sintomi di interessamento del motoneurone superiore (primo motoneurone) e inferiore (secondo motoneurone) siano presenti in regioni corporee non contigue, intendendo per regioni i distretti bulbare, cervicale, toracico e lombosacrale.
Terapia
Dal punto di vista terapeutico l’unico farmaco attualmente (2010) dimostratosi utile è il riluzolo, che agisce come inibitore del rilascio presinaptico del glutammato (dose massima di 100 mg/die) e che aumenta la sopravvivenza di circa tre mesi. Ciò che migliora la qualità della vita nei malati di SLA è l’approccio multidisciplinare che agisce mediante il trattamento sintomatico del dolore, dell’eccessiva salivazione (scialorrea), della labilità emotiva, della spasticità, ecc.; oltre alle cure palliative si possono rendere necessari il supporto alla respirazione (ventilazione non invasiva o tracheotomia) e alla nutrizione (suggerimenti nutrizionali e nutrizione artificiale) e aiuti alla comunicazione e alla motricità.