neurogenesi
neurogenesi
Processo attraverso il quale vengono generati nuovi neuroni da cellule immature. Si possono distinguere due tipi di n.: la n. durante lo sviluppo, che dà origine alle cellule nervose e gliali destinate a formare i tessuti del sistema nervoso, e la n. dell’adulto, il cui significato è legato alla plasticità funzionale di determinate aree cerebrali.
Neurogenesi durante lo sviluppo
Dopo la formazione del tubo neurale (➔ cervello, sviluppo del), lo strato di cellule che si trova a contatto con la cavità dei ventricoli va incontro a cicli di proliferazione da cui derivano tutti i neuroni e le cellule della glia. Inizialmente, le cellule progenitrici si dividono in modo simmetrico, generando altre cellule progenitrici. In seguito, cicli di divisioni asimmetriche danno origine alla nascita di altre cellule progenitrici e di neuroni che escono dal ciclo cellulare e migrano a lunga distanza, raggiungendo la loro posizione finale nel cervello e nel midollo spinale. I neuroni si moltiplicano con un ritmo di circa 4.000 al secondo e, al termine della 16a settimana, sono più di 20 miliardi. Questo processo conduce alla formazione di una zona ventricolare che contiene le cellule proliferative, una zona intermedia che contiene assoni e neuroni in migrazione, e la cosiddetta zona della preplacca che contiene i precursori neuronali postmitotici. Più tardivamente, tra la zona ventricolare e la zona intermedia si costituisce una seconda regione di cellule mitoticamente attive, denominata zona subventricolare, a livello della quale si formano zone germinali secondarie (➔ differenziamento neuronale).
Neurogenesi nell’adulto
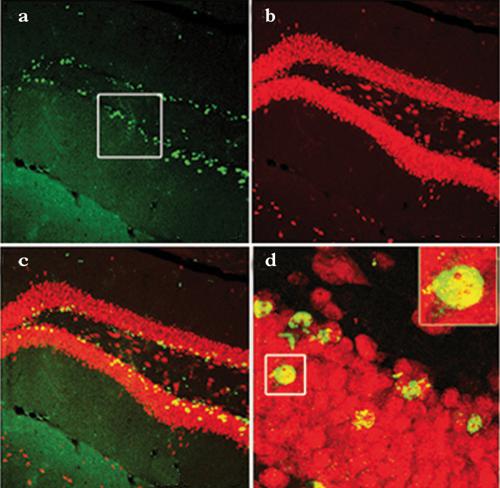
Come dimostrato dagli studi pioneristici di Joseph Altman e, successivamente, di Fred H. Gage, nel cervello adulto dei mammiferi la n. permane a livello della zona subgranulare del giro dentato dell’ippocampo e della zona subventricolare dei ventricoli laterali. In queste zone, infatti, è stata dimostrata la presenza di cellule staminali neuronali, definite a livello funzionale come cellule capaci di autorinnovamento e multipotenti, cioè in grado di differenziarsi in numerose linee neuronali, quali i neuroni, gli astrociti e gli oligodendrociti.
Le cellule staminali neuronali dell’ippocampo danno origine ai neuroni eccitatori granulari, mentre le cellule dei ventricoli laterali migrano lungo la via migratoria rostrale (rostral migratory stream) e si differenziano negli interneuroni inibitori dei bulbi olfattivi. Anche negli uccelli il cervello adulto presenta n., in partic. nelle specie canore studiate dal gruppo di Fernando Nottebohm, nelle quali, sotto l’azione del testosterone, si attiva una cascata molecolare che, attraverso l’azione del fattore VEGF (Vascular Endotelial Growth Factor) delle cellule endoteliali dei capillari cerebrali e del fattore BDNF (Brain Derived Neurotrophic Factor), promuove la produzione e il reclutamento di nuovi neuroni nei centri vocali superiori. Pertanto, il sistema vascolare e le cellule staminali neuronali sono funzionalmente e anatomicamente accoppiati a livello di una struttura specializzata, chiamata nicchia vascolare neurogenica, che costituisce un microambiente locale dove le cellule staminali dell’adulto interagiscono con segnali ambientali tramite l’intermediazione di fattori rilasciati dai vasi sanguigni e dagli astrociti della nicchia stessa. Analogamente, la n. e l’angiogenesi (formazione di nuovi vasi sanguigni) sono due processi paralleli e reciprocamente regolati. Al di fuori dell’ippocampo e del sistema olfattivo, la n. appare estremamente limitata o assente nell’individuo sano. Tuttavia, in seguito a processi patologici, quali danni ischemici, epilessia e malattie degenerative, altre aree del sistema nervoso centrale possono diventare attivamente neurogeniche. Il significato funzionale della n. dell’adulto è incerto. È comunque provato che la distruzione delle cellule staminali ippocampali (a seguito di irradiazione) produce una riduzione delle performance comportamentali dipendenti da quest’area, come evidenziato in compiti di memoria spaziale. Parimenti, l’esercizio intensivo in alcuni di questi compiti stimola potentemente la n. ippocampale. È di grande interesse la dimostrazione che stimoli ambientali diversi agiscono a livelli differenti nella regolazione degli eventi della n.: mentre l’esercizio fisico volontario (soprattutto la corsa) promuove la proliferazione dei precursori neuronali, gli stimoli cognitivi e l’apprendimento promuovono la sopravvivenza e il reclutamento delle cellule neoformate. Nel suo insieme, la stimolazione ambientale induce modificazioni plastiche nel cervello che, perdurando nel tempo, possono aumentare la riserva cognitiva dell’individuo, cioè la capacità di recuperare da danni cerebrali dovuti a traumi o malattie neurodegenerative o di contrastare gli effetti dell’invecchiamento (➔ ambiente e cervello).
Ruolo del BDNF nella neurogenesi dell’adulto
La via del BDNF e del suo recettore cellulare (TrkB) ha un ruolo chiave nella regolazione della n. del cervello adulto. Lo stress, un fattore che può causare la depressione o altri disturbi dell’umore, riduce i livelli di BDNF e di n. nell’ippocampo. In animali stressati trattati con farmaci antidepressivi, invece, i livelli di BDNF e di n. aumentano. Inoltre, l’infusione di BDNF nella zona subgranulare del giro dentato dell’ippocampo stimola la n. e ha mostrato una spiccata azione antidepressiva in numerosi test comportamentali. Analogamente, condizioni che aumentano i livelli di BDNF, quali l’esercizio fisico, la restrizione calorica e l’esposizione a una vita ricca di stimoli motori, sensoriali e cognitivi (ambiente arricchito), innalzano notevolmente i livelli di n. nell’ippocampo. Il BDNF è anche importante per la n. del bulbo olfattivo. L’iniezione di BDNF nella zona subventricolare dei ventricoli laterali, infatti, aumenta i livelli di n. e può indurre processi neurogenici ectopici nello striato e nell’ipotalamo.