La grande scienza. Dinamica dei reagenti complessi sistemi
La grande scienza. Dinamica dei reagenti complessi sistemi
Dinamica dei sistemi reagenti complessi
La chimica contemporanea costituisce un efficace e spesso indispensabile strumento per la comprensione dei fenomeni naturali, inclusi quelli riguardanti le scienze della vita. Essa non solo occupa un ruolo di primo piano nella progettazione e nello sviluppo di tecnologie avanzate ma offre anche la possibilità di affrontare problemi di frontiera della ricerca scientifica, alcuni dei quali ricchi di implicazioni filosofiche. A tale proposito, è sufficiente osservare come le ricerche sull'origine della vita non possano prescindere da un'adeguata e profonda conoscenza dei meccanismi attraverso i quali i sistemi macromolecolari si autoorganizzano per acquisire ben definite funzionalità. Non solo: le recenti scoperte, realizzate per via spettroscopica, sulla presenza di composti organici nelle nubi cosmiche, sempre ritenute inospitali per le molecole (anche perché percorse da radiazioni di elevata energia), sembrano offrire enormi prospettive per lo studio di tale fondamentale problematica.
Una delle principali linee di evoluzione della ricerca chimica moderna riguarda la descrizione dei sistemi complessi di molecole, nella quale la chimica interagisce strettamente con altre discipline quali la fisica, la scienza dei materiali e la biologia. La natura dei problemi affrontati è assai varia: si va dalle complesse sequenze di reazioni che intervengono nei processi biologici, alla distribuzione dei gas serra nell'atmosfera e ai processi di autoorganizzazione attraverso i quali emergono spontaneamente configurazioni molecolari con un grado di ordine superiore a quello della miscela originaria. Tutto ciò in un'impostazione dinamica nella quale la velocità con cui hanno luogo i singoli eventi molecolari gioca un ruolo di primaria importanza nella descrizione dell'evoluzione del sistema globale.
Le acquisizioni conseguite nel settore delle scienze molecolari hanno conferito alla chimica contemporanea la capacità di affrontare con confidenza e affidabilità problematiche che coinvolgono la conoscenza dettagliata della struttura della materia e delle trasformazioni cui essa è soggetta. Tutto ciò sulla base di una successione gerarchica di eventi che procedono dal livello microscopico a quello macroscopico in un vertiginoso passaggio di scala di dieci ordini di grandezza, vale a dire dalle dimensioni atomiche a quelle ordinarie. I risultati che si ottengono con questo approccio offrono i criteri per la descrizione e la modellazione di fenomeni e processi di vario interesse. Inoltre, essi costituiscono un prezioso orientamento nell'esplorazione di fenomeni la cui analisi sperimentale presenta talora difficoltà, per esempio nei settori riguardanti le sintesi condotte a elevate temperature, la combustione, la preparazione di nuovi materiali, la chimica atmosferica e la chimica dei processi biologici. Un altro campo che recentemente ha suscitato notevole interesse è la cosmochimica, disciplina che si occupa di studiare la natura, la formazione e la trasformazione dei composti chimici presenti nelle nubi cosmiche.
Tra gli aspetti più ricchi di implicazioni, vi è l'evidenza che dal comportamento dinamico dei sistemi chimici complessi possano emergere strutture ordinate e coerenti nel tempo e nello spazio, o autoorganizzate, in apparente contrasto con quanto previsto dal secondo principio della termodinamica, che privilegia il decadimento verso il disordine.
Lo scopo di questo saggio è illustrare i metodi e le strategie di approccio usati per affrontare tali problemi, evidenziando in particolare come la loro analisi permetta di giustificare l'insorgenza delle menzionate strutture spazio-temporali coerenti e quindi ordinate. Successivamente verranno illustrati a titolo esemplificativo alcuni problemi specifici che riguardano rispettivamente la preparazione dei materiali per la cristallizzazione e la dinamica dei processi metabolici, nei quali l'insieme delle reazioni coinvolte risulta opportunamente coordinato per garantire la sopravvivenza e la replicazione dei sistemi cellulari.
Sistemi complessi di reazioni
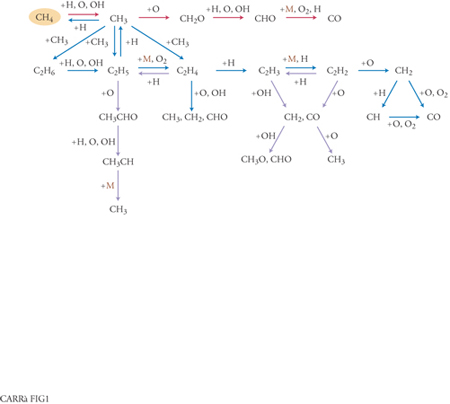
Gran parte delle trasformazioni chimiche avviene mediante un insieme anche molto numeroso di trasformazioni semplici dette 'elementari', che si sovrappongono e si incrociano dando origine a una rete di connessioni di elevata complessità. Per esempio, se si fa interagire l'ossigeno con l'idrocarburo più semplice, il metano, ha luogo una trasformazione che in particolari condizioni diviene rapidissima, al limite esplosiva, e che globalmente porta alla formazione di acqua e anidride carbonica. Questo processo, apparentemente semplice, coinvolge in realtà decine di composti chimici che interagiscono attraverso una complessa rete di reazioni elementari, alcune delle quali sono illustrate nella fig. 1. Uno degli obiettivi dell'industria chimica è proprio quello di controllare tali reazioni, operando in condizioni blande e in presenza di opportuni catalizzatori, in modo da poter isolare specie intermedie che si prestino a opportune applicazioni.
Come è noto, anche l'energia necessaria per alimentare le trasformazioni che avvengono negli organismi viventi viene prodotta da un processo di 'combustione', attraverso il quale le sostanze nutritive (per es., l'amido) vengono trasformate in anidride carbonica e acqua. Anche in questo caso interviene un ciclo complesso di reazioni, il ciclo di Krebs, del tutto diverso dal precedente poiché si verifica in una soluzione acquosa, a temperatura ordinaria e con una velocità globale bassa, compatibile con quella degli altri processi che hanno luogo negli organismi viventi. Si tratta di processi nei quali intervengono in modo essenziale gli enzimi, importantissimi catalizzatori bioorganici di natura proteica.
Nell'ambito di un'impostazione riduzionistica l'analisi e la simulazione dei processi menzionati può essere perseguita attraverso la determinazione dei parametri cinetici, che condizionano la velocità delle trasformazioni elementari in gioco e che perciò possono essere successivamente utilizzati nella descrizione del sistema globale. Al fine di perseguire tale obiettivo è necessario evidenziare le caratteristiche strutturali e dinamiche dei cosiddetti 'complessi attivati', configurazioni instabili derivanti dalla collisione di molecole diverse, che giocano un ruolo determinante sulla velocità delle reazioni elementari. Recentemente Ahmed H. Zewail, premio Nobel per la chimica nel 1999, attraverso l'impiego della spettroscopia basata su impulsi laser molto brevi, dell'ordine dei femtosecondi (10−15 s), è riuscito a determinare sperimentalmente le caratteristiche geometriche di alcuni complessi attivati. Infatti colpendo particolari molecole con impulsi di due diversi laser è possibile 'fotografare' il momento preciso in cui si rompono i legami fra alcuni atomi e se ne formano nuovi.
Parallelamente alle indagini sperimentali, anche gli studi teorici contribuiscono ad approfondire la conoscenza di questi aspetti dei sistemi reattivi. La teoria della velocità delle reazioni chimiche era già stata formulata nella prima metà del secolo scorso, tenuta a battesimo da scienziati di rilievo, quali Eugene Wigner, Cyril N. Hinshelwood, Henry Eyring e Michael Polanyi. Purtroppo, una sua adeguata e soddisfacente applicazione era destinata a essere procrastinata, a causa della mancanza dei mezzi di calcolo per poterla perseguire. Il recente sviluppo delle scienze e delle tecnologie informatiche ha portato alla costruzione di calcolatori di potenza così elevata da rendere superabili le difficoltà che per anni hanno frustrato i pionieri della chimica teorica. Si intravede ormai la possibilità di formulare la chimica su basi quantitative e predittive mediante la soluzione delle equazioni della meccanica quantistica. Per perseguire questo scopo si deve affrontare lo spinoso problema del calcolo dell'energia di sistemi molecolari costituiti da più nuclei atomici e dall'insieme di elettroni che gravitano attorno a essi, soggetti a interazioni coulombiane a lungo raggio. Tale calcolo va eseguito per diversi valori delle variabili spaziali che individuano le posizioni dei nuclei, in modo da ottenere l'andamento dell'energia in funzione di queste (le cosiddette 'superfici di energia potenziale'). Attualmente è possibile calcolare, almeno per molecole relativamente piccole, le superfici di energia potenziale che descrivono le interazioni fra le molecole che collidono dando luogo a una reazione chimica. Risulta così possibile descrivere l'evoluzione di un sistema molecolare nel passaggio dai reagenti ai prodotti di reazione; studiando la dinamica dei moti atomici su tali superfici si descrive la rottura di alcuni legami e la formazione di altri. La capacità di costruire le superfici di energia potenziale mediante il calcolo ha aperto un'ampia finestra sul mondo della dinamica chimica, offrendo la possibilità di prevedere il percorso seguito dalle reazioni. Tra l'altro, diviene così possibile avventurarsi nella descrizione di eventi reattivi che hanno luogo in condizioni estreme di temperatura e pressione, non facilmente realizzabili in laboratorio.
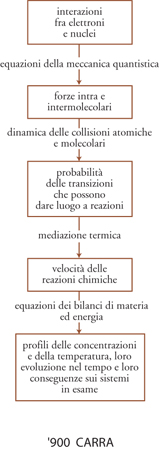
In conclusione, lo studio della dinamica dei sistemi reagenti può essere perseguito attraverso una successione gerarchica di eventi che procede dalle variabili microscopiche a quelle macroscopiche seguendo lo schema della fig. 3. Questa impostazione contempla una transizione dalle dimensioni atomiche, corrispondenti a 10−8 cm, a quelle ordinarie che ammontano a decine di centimetri. Lo schema precedente vale naturalmente sia per processi che avvengono in una miscela gassosa sia per reazioni che hanno luogo nei sistemi condensati, in particolare nelle soluzioni liquide. In quest'ultimo caso il processo di mediazione termica coinvolge ovviamente anche le molecole del solvente che si trovano a stretto contatto con i reagenti.
Approccio sintetico allo studio dei sistemi reagenti complessi
La menzionata complessità di gran parte dei sistemi reagenti presenti in Natura pone spesso limitazioni notevoli a un'analisi nella quale si voglia tenere esplicitamente conto di tutti i fenomeni elementari in essi coinvolti. In realtà questo approccio appare per alcuni aspetti 'retorico' poiché solo raramente si dispone di informazioni tali da potere conseguire una descrizione così dettagliata. Inoltre, non sempre risulta necessario, poiché il più delle volte solo alcune delle reazioni in gioco condizionano l'evoluzione del sistema e la velocità del processo globale. Infatti, poiché ciascuna reazione è caratterizzata da una particolare velocità che dipende dalle condizioni operative e dall'ambiente, finiscono per prevalere quei processi reattivi che risultano più agevoli dal punto di vista cinetico. Si apre pertanto il problema di individuare tali reazioni in modo da poter semplificare gli schemi cinetici senza perdere le caratteristiche peculiari del sistema in esame. In tale impostazione il sistema viene dunque descritto attraverso alcune reazioni significative e utilizzando valori apparenti dei parametri cinetici che ne caratterizzano il comportamento in corrispondenza di una particolare scala temporale, spaziale o termica. Pur trattandosi di un procedimento per alcuni aspetti rinunciatario e per altri aleatorio, esso presenta una indiscutibile utilità quando si sappiano cogliere gli effetti chimici e fisici che determinano i processi in gioco, individuando con chiarezza l'obiettivo da perseguire.
Per esempio, la menzionata reazione di combustione del metano, che, come abbiamo visto, si svolge attraverso un numero molto elevato di composti intermedi presenti in piccola concentrazione, può essere descritta in prima approssimazione mediante una reazione globale che trasforma il metano in anidride carbonica e acqua, trascurando la presenza delle altre specie. Questo tipo di approccio è sicuramente utile se siamo interessati a valutare la quantità di energia che si libera nel processo di combustione, ma diviene inadeguato qualora si voglia valutare la formazione di composti inquinanti, quali gli ossidi di azoto, favorita dalla presenza di intermedi radicalici. Questi ultimi, pur essendo presenti in quantità apparentemente trascurabili, finiscono per giocare un ruolo importante quando si ponga l'attenzione sui problemi connessi al controllo ambientale. Fenomeni di questo tipo giustificano l'intensificarsi di ricerche che, attraverso l'impiego di metodologie diagnostiche molto sofisticate basate sull'uso del laser, siano in grado di individuare specie presenti in concentrazioni molto basse.
Nella trattazione che segue ci riferiremo a sistemi reagenti aperti, identificando una zona dello spazio in corrispondenza della quale siano presenti flussi di materia entranti e uscenti, che contengono rispettivamente i reagenti e i prodotti di reazione. In condizioni stazionarie la somma dei flussi entranti uguaglia quella dei flussi uscenti e i valori delle diverse concentrazioni si mantengono inalterati nel tempo. In generale però il sistema è soggetto a un'evoluzione dinamica in virtù della quale ha luogo un accumulo o un depauperamento di alcuni composti. Rientrano in tale tipologia molti e differenziati sistemi naturali e industriali che comprendono, per esempio: l'atmosfera, che costituisce una vera e propria 'zuppa' chimica per la presenza di componenti che, pur essendo presenti in quantità minime, interagendo fra loro possono portare a evoluzioni indesiderate; le cellule, nelle quali si intrecciano le diverse reazioni enzimatiche che stanno alla base del loro metabolismo, nonché del loro controllo e sviluppo; il cosiddetto 'brodo prebiotico', nel quale attraverso l'interazione di diversi componenti chimici si sono manifestate interessanti proprietà emergenti che hanno favorito la formazione di strutture molecolari ordinate; le unità industriali nelle quali si realizzano le sintesi chimiche e le unità di produzione di energia attraverso processi di combustione.
Prima di esaminare alcuni esempi specifici, è importante sottolineare come anche attraverso un'analisi semplificata che coinvolge un numero limitato di reazioni sia possibile evidenziare alcuni comportamenti peculiari dei sistemi reagenti che si manifestano attraverso l'insorgenza di 'strutture' le quali possono essere o ordinate nel tempo e nello spazio o irregolari e caotiche. L'esempio più noto è costituito dalla reazione di Belousov-Chabotinsky, nella quale ha luogo l'ossidazione di un acido organico, per esempio l'acido maleico, in presenza di bromati alcalini e sali di cerio in una soluzione acida. Nel corso di questa reazione si manifesta un'oscillazione nel tempo della concentrazione dello ione cerio nei suoi diversi stadi di ossidazione, accompagnata da tipici effetti cromatici. Anche se il meccanismo dettagliato della reazione non è ancora ben noto, sono sicuramente presenti effetti dovuti a retroazioni autocatalitiche in virtù delle quali uno dei prodotti di reazione influenza la velocità di una delle reazioni che hanno portato alla sua formazione. La presenza simultanea delle reazioni autocatalitiche e della diffusione dei reagenti può dare origine a un ordine spazio-temporale: per esempio, se la reazione viene condotta su un film liquido si formano onde che si propagano come illustrato nella fig. 4.
Dal punto di vista matematico tali sistemi vengono descritti mediante equazioni differenziali del secondo ordine alle derivate parziali non lineari. Esse riflettono i bilanci di materia riferiti ai diversi componenti, che tengono conto degli effetti dovuti alle reazioni chimiche e alla diffusione. La non linearità è presente nell'espressione della velocità di reazione e costituisce un requisito indispensabile perché si possano manifestare gli effetti menzionati. Essa consegue dal fatto che dal punto di vista microfisico una reazione chimica il più delle volte trae origine dall'incontro di due molecole e poiché la probabilità dell'evento è proporzionale al prodotto delle concentrazioni delle sostanze reagenti, la sua velocità risulterà espressa da una relazione matematica di tipo quadratico. Una ulteriore fonte di non linearità si riscontra nell'influenza della temperatura sulla velocità di reazione. La legge che regola tale dipendenza si può infatti esprimere con una relazione non lineare che, rappresentata graficamente, presenta un tipico andamento a 'esse'. La non linearità ha costituito sino a qualche anno fa un enorme ostacolo per chi era impegnato nello studio dell'evoluzione nel tempo di sistemi soggetti a reazioni chimiche, poiché impedisce di ottenere la soluzione analitica delle equazioni di bilancio. Lo sviluppo dei calcolatori ha cambiato il panorama in modo significativo poiché ha reso possibile la soluzione per via numerica delle equazioni differenziali della dinamica chimica.
La presenza di andamenti oscillanti nel tempo e nello spazio delle concentrazioni delle diverse specie in gioco rivela l'emergenza di fenomeni di autoorganizzazione. Questa possibilità era stata anticipata da Alan M. Turing nel 1952 in un lavoro pionieristico nel quale veniva evidenziato che lo sviluppo di strutture spaziali deriva da perturbazioni cui è soggetto il sistema reagente stesso, quali, per esempio, fluttuazioni di concentrazione o temperatura. Esse danno luogo a una rottura di simmetria in virtù della quale in un mezzo uniforme, e quindi del tutto simmetrico, si generano configurazioni spazio-temporali meno simmetriche ma più ordinate. L'intento di Turing era di giustificare i processi morfogenici che si manifestano nei sistemi biologici, attribuiti all'effetto esercitato da opportune sostanze chimiche chiamate 'morfogeni' sulla velocità delle reazioni biochimiche presenti nel sistema. È curioso segnalare che Turing aveva tratto ispirazione da una figura inclusa in un libro per ragazzi dal titolo Natural wonders every child should know, che descrive i primi stadi del processo di gastrulazione di una cellula-uovo fecondata.
Come si è visto, affinché possano verificarsi tali processi morfogenici è necessario che abbiano luogo reazioni chimiche la cui velocità dipende in modo non lineare dalle concentrazioni dei reagenti, associate alla diffusione di alcuni componenti. Un esempio interessante, e molto studiato, è quello in cui è presente un meccanismo di retroazione autocatalitico nel quale uno dei componenti di una serie di reazioni successive influisce sul comportamento di una delle reazioni che precede la sua formazione, aumentandone o diminuendone la velocità. Questi effetti di attivazione e inibizione possono interagire reciprocamente ed essere modulati dalla differenza fra la velocità di diffusione dei componenti stessi. Hanno così luogo processi di reazione-diffusione che portano alla formazione di intricate distribuzioni delle concentrazioni spazialmente non uniformi. I risultati così ottenuti sembravano limitati a sistemi non viventi poiché i comuni schemi catalitici biosintetici tendono tipicamente a non esaltare la velocità. Questa riserva è stata però rimossa dalla scoperta di alcuni fattori biosintetici autoesaltanti quali, per esempio, alcune proteine regolatrici di geni. La fig. 6 illustra una loro possibile applicazione, descrivendo il risultato della simulazione dello sviluppo del profilo oscillante della concentrazione di una specie morfogena. Questo andamento potrebbe indurre la formazione di aggregazioni cellulari che precedono a loro volta le differenziazioni di cartilagini che stanno alla base della formazione di strutture scheletriche articolate presenti negli organismi viventi.
La formazione spontanea di configurazioni ordinate potrebbe sembrare in contrasto con il secondo principio della termodinamica, che sancisce la tendenza dei sistemi naturali a evolvere verso configurazioni sempre più disordinate, espressa quantitativamente dall'aumento nel tempo dell'entropia. In realtà, poiché le trasformazioni avvengono in sistemi aperti, se i flussi di materia ed energia entranti sono associati a un basso contenuto entropico specifico e quelli uscenti a un elevato contenuto entropico, nell'ambito del sistema può avere luogo una diminuzione locale di entropia compatibilmente con la formazione di strutture ordinate come quelle menzionate.
L'interpretazione dei processi morfogenetici biologici condotta su basi puramente chimico-fisiche comprende, oltre ai fattori sin qui illustrati, del tipo reazione-diffusione, una classe ampia di fenomeni nei quali intervengono altri fattori fisici, come la separazione tra fasi liquide diverse, la tensione superficiale, gli effetti gravitazionali e la viscosità. Essi si contrappongono agli effetti dominati da fattori genetici che stanno alla base dei processi di sviluppo, condizionati da interazioni altamente organizzate tra macromolecole specifiche.
Crescita cristallina
I processi di formazione, o meglio di crescita, di un cristallo a partire da un gas o da un liquido sono noti e studiati da lungo tempo. In questi studi convergono conoscenze che fanno capo a settori disciplinari molto diversi, che vanno dalla termodinamica alla dinamica dei fluidi, includendo molti aspetti della cinetica delle reazioni chimiche. Questo approccio multidisciplinare ha evidenziato come, attraverso il controllo di alcuni parametri macroscopici quali la concentrazione delle specie presenti nel fluido e coinvolte nella deposizione, la temperatura, la velocità del fluido, sia possibile determinare le caratteristiche strutturali e morfologiche del solido che viene ottenuto.
Lo scopo di questa trattazione non è quello di esaminare esaustivamente la tipologia dei processi di crescita, ma di soffermarsi su due di essi: la deposizione chimica da una fase vapore e la crescita da una soluzione. Il primo viene indicato con l'acronimo CVD (chemical vapor deposition) e costituisce attualmente un processo largamente usato su scala industriale per la preparazione di materiali, in particolare il silicio, impiegati nella costruzione di dispositivi elettronici. Le sue caratteristiche microscopiche sono illustrate nella fig. 7 mediante un modello di crescita detto 'a gradini e terrazze', introdotto in The growth of crystals and the equilibrium structure of their surfaces (1951) di W.K. Burton, N. Cabrera e F. C. Frank. La sua validità è stata recentemente confermata dalle immagini ottenute mediante la microscopia a scansione a effetto tunnel (STM, scanning tunnelling microscopy) che, come illustrato nella fig. 7, evidenziano l'esistenza di una crescita a strati, mediante la deposizione di atomi sulle terrazze che individuano la superficie del solido, lungo le quali gli atomi diffondono sino a raggiungere un gradino, contribuendo così alla sua crescita. Nella fig. 7A viene illustrato come questo processo di crescita avvenga attraverso un insieme di stadi cinetici che ha inizio con il trasporto alla superficie del solido (per diffusione) della specie gassosa che dà luogo alla deposizione; qui, mediante una trasformazione chimica, vengono liberati gli atomi del componente solido che successivamente diffondono sulla superficie.
Molto spesso il processo coinvolge diverse trasformazioni chimiche che avvengono non solo sulla superficie del solido ma anche nel gas (la fig. 8 si riferisce alla deposizione di silicio da silano, SiH4). Sebbene si tratti di un processo apparentemente semplice, globalmente rappresentato dalla reazione SiH4→Si+2H2, ancora una volta sono coinvolte diverse specie. La descrizione della sua dinamica è pertanto fondamentale per poter individuare le condizioni operative che permettono di ottenere un materiale con caratteristiche desiderate: un monocristallo, un policristallo o un solido amorfo, privo di struttura cristallina ordinata. Infatti, se la velocità delle trasformazioni chimiche superficiali, estremamente sensibile alla temperatura, è elevata rispetto a quella della diffusione superficiale degli atomi, questi tendono a formare grappoli o 'cluster' superficiali che favoriscono la formazione di un policristallo, al limite di un solido amorfo. D'altro canto la velocità del gas che lambisce la superficie influenza quella di trasporto del componente attivo dal cuore della fase gassosa alla superficie del solido. Se questo stadio è sufficientemente lento da limitare la velocità del processo globale, gli atomi depositati sulla superficie possono agevolmente diffondere per occupare le posizioni che competono loro in una struttura regolare monocristallina. Pertanto, agendo sui parametri operativi risulta possibile controllare le caratteristiche del materiale che si vuole ottenere. In questo quadro risulta di particolare interesse tecnologico la cosiddetta 'crescita epitassiale' nella quale la deposizione avviene su una superficie monocristallina che guida l'orientazione cristallografica del deposito stesso. Si ottengono così materiali monocristallini dai quali si preparano i microchip utilizzati nella fabbricazione dei dispositivi elettronici.
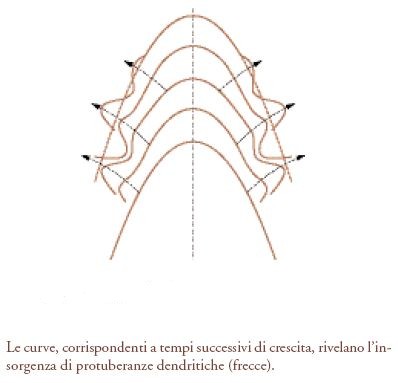
La crescita di un componente presente in una soluzione liquida fornisce gli esempi più belli e familiari di cristalli naturali aventi le cosiddette strutture dendritiche, con propaggini a forma di dita. Esse presentano una caratteristica forma ad albero illustrata nella fig. 9, dove viene evidenziata la crescita del cristallo nel tempo.
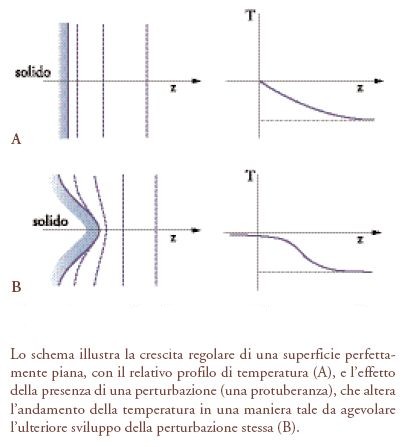
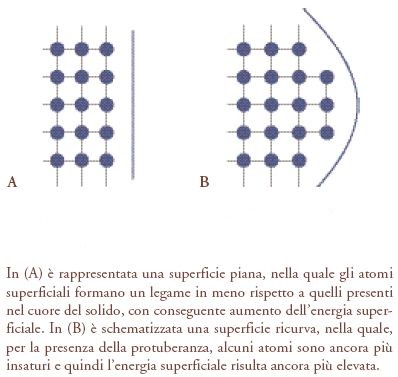
Per approfondire le caratteristiche dei processi di cristallizzazione che portano alla formazione di strutture dendritiche, è opportuno osservare che non esiste un meccanismo interno che controlla il processo, per cui si deve assumere che esso sia condizionato dall'ambiente esterno. Lo studio della dinamica del processo di solidificazione dell'acqua è stato intrapreso per la prima volta, alla fine dell'Ottocento, da Josef Stefan, che si era proposto di valutare la velocità di crescita di un iceberg. A una prima analisi si può prevedere che la solidificazione avvenga in modo tale che la superficie piana del solido mantenga la sua configurazione spostandosi, durante la crescita, parallelamente a sé stessa. Sulla superficie solida la temperatura è leggermente superiore a quella dell'acqua con cui essa è a contatto (fig. 10) poiché il processo avviene in condizioni di non equilibrio termodinamico e localmente si libera il calore di solidificazione dell'acqua. Questa differenza di temperatura costituisce la forza motrice del processo, poiché la velocità con cui avviene lo scambio fra il solido e il liquido del calore liberato nel processo di solidificazione è proporzionale a essa. Se la superficie del solido non è piana si manifesta su di essa un accumulo locale di energia dovuto all'influenza della sua curvatura sulla insaturazione degli atomi superficiali, come illustrato nella fig. 11. Ciò fa sì che la differenza locale di temperatura fra il solido e il liquido a contatto assuma un valore massimo in corrispondenza della sommità della protuberanza. Ne consegue che se, per effetto di una fluttuazione di temperatura o dell'esistenza di un'imperfezione cristallina, si forma una protuberanza come quella illustrata nella fig. 10B, l'andamento della temperatura nel passaggio dal solido al liquido risulta alterato rispetto a quello di una superficie piana, illustrato nella fig. 10A. La presenza di una più elevata differenza di temperatura aumenta la velocità di dispersione del calore di solidificazione e, di conseguenza, la velocità di crescita in corrispondenza della protuberanza. In realtà l'entità del processo dipende dalla competizione fra l'effetto destabilizzante che aumenta con la velocità di crescita e quello stabilizzante dovuto all'aumento dell'energia interfacciale che tende a contrastare le deviazioni dalla planarità. Se prevale il primo effetto, il sistema cresce indefinitamente dando origine alla formazione di una branca dendritica. Studiando l'evoluzione di una struttura a punta, come illustrato nella fig. 12, risulta possibile simulare la formazione di una struttura dendritica simile a quella della fig. 9.
Modelli di comportamento e di diversificazione cellulare
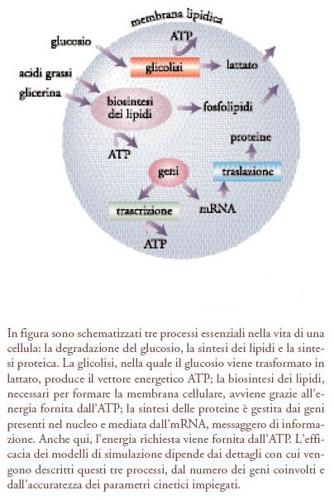
Nella biologia molecolare sono ancora sporadici i modelli quantitativi simili per generalità, compattezza ed eleganza a quelli familiari ai fisici. Essi non si sono ancora riscattati da un carattere empirico, strettamente ancorato alle informazioni ottenute dalle osservazioni sperimentali. Tuttavia, da alcuni anni sta maturando la consapevolezza che esista una concreta possibilità di formulare modelli cellulari che, pur fruendo dei risultati delle esperienze, contribuiscano non solo ad aumentare le nostre conoscenze sul comportamento dei sistemi cellulari ma anche a prevederlo in presenza di sollecitazioni esterne. Le ragioni di questo ottimismo risiedono sia nell'aumento delle informazioni che si stanno acquisendo sui meccanismi enzimatici che sono alla base dei processi biologici, sia nella disponibilità di calcolatori sempre più potenti che offrono la possibilità di risolvere con accuratezza i complessi sistemi di equazioni differenziali che esprimono i bilanci di materia dei diversi componenti. L'obiettivo è quello di esplorare gli effetti che possono emergere dall'interazione di diverse reazioni che singolarmente non darebbero luogo a comportamenti particolari. Vengono così costruiti modelli cellulari virtuali (in silico) che, fruendo delle conoscenze sperimentali sul modo in cui le molecole diffondono e reagiscono nelle cellule, evidenziano il comportamento di alcuni componenti cellulari. Nella fig. 13 sono schematizzati i principali processi biochimici interni a una cellula, che riguardano in particolare tre aspetti fondamentali del suo metabolismo: (1) quello energetico, attraverso la demolizione del glucosio con formazione di ATP, il vettore energetico o 'carburante' degli altri processi; (2) quello strutturale, attraverso la sintesi dei lipidi che autoassemblandosi formano la membrana cellulare; (3) quello del controllo e dello sviluppo, che avviene attraverso la sintesi delle proteine gestita dai geni, depositari del patrimonio di informazioni contenute nella cellula. Le proteine, a loro volta, sono responsabili di molte attività funzionali che caratterizzano il livello organizzativo della cellula.
La formulazione di questi modelli costituisce un settore di indagine in fase di sviluppo, in piena sinergia con la rapida evoluzione dei calcolatori e delle tecniche sperimentali, che permettono di acquisire dati sempre più accurati. Come menzionato, le aspettative di queste ricerche sono essenzialmente volte alla messa a punto di strumenti utili per l'analisi e la simulazione del comportamento del materiale biologico sottoposto a perturbazioni esterne, soprattutto in condizioni non facilmente realizzabili sperimentalmente. Purtroppo la complessità delle cellule è tale da richiedere la costruzione di modelli molto sofisticati, tanto che, nonostante i recenti progressi, non si è ancora riusciti a formulare descrizioni capaci di coglierne tutti gli aspetti essenziali. Per questa ragione, il problema della dinamica evolutiva di un sistema di cellule viene affrontato anche con modelli più semplici, che comprendono alcuni aspetti essenziali riguardanti i processi di crescita e di divisione.
Un approccio interessante è basato sull'ipotesi che in ciascuna cellula, protetta dall'ambiente da una membrana permeabile solo ad alcuni componenti, abbia luogo un insieme di reazioni collettivamente autocatalitiche. Senza specificare la natura delle sostanze reagenti, è sufficiente osservare che si tratta di composti aventi il comportamento chimico tipico delle sostanze coinvolte nei processi metabolici. Le interazioni fra le diverse cellule avvengono attraverso l'ambiente circostante, nel quale le concentrazioni delle sostanze sono soggette a fluttuazioni dovute ai moti browniani. In sostanza, ciascuna cellula viene assimilata a un reattore aperto ai flussi di materia con l'esterno in modo da poter ricevere le sostanze nutrienti ed eliminare alcuni prodotti delle reazioni. Quando la concentrazione di uno o più costituenti supera una determinata soglia, la cellula si divide. Viceversa, alcune cellule possono morire per difetto di nutrimento. In questa impostazione la differenziazione e l'evoluzione cellulare emergono dalla dinamica dei processi precedentemente descritti. Le equazioni che esprimono il bilancio di materia dei diversi componenti contengono, oltre ai termini cinetici relativi alle reazioni chimiche in gioco, anche quelli associati al loro trasporto attraverso la membrana, e un ulteriore termine che riflette l'influenza delle menzionate fluttuazioni di concentrazione. Si riscontra allora che la non linearità delle equazioni così formulate dà luogo a un andamento oscillante delle concentrazioni dei diversi componenti presenti nelle cellule. Ciò fa emergere uno scenario particolarmente interessante per la descrizione dell'evoluzione di una società di cellule. Esso è riassunto nella fig. 14 mediante i diagrammi ormai tipici della dinamica dei sistemi complessi, che fanno uso dello spazio delle fasi. In questi diagrammi si rappresenta sugli assi coordinati la concentrazione dei componenti chimici cellulari (nell'esempio illustrato ci si è limitati per semplicità a tre componenti); ciascun diagramma corrisponde a valori diversi del tempo. La presenza di traiettorie che ritornano su sé stesse è appunto caratteristica di un processo oscillatorio.
L'aspetto peculiare che emerge dalle simulazioni numeriche è costituito dal fatto che le oscillazioni di composizione sono inizialmente sincrone fra le diverse cellule; con il procedere delle divisioni interviene una rottura della simmetria che si manifesta con la presenza di due gruppi di cellule aventi valori diversi delle fasi delle oscillazioni. Successivamente le cellule con fasi diverse subiscono ulteriori divisioni che contribuiscono a differenziarne ulteriormente la composizione. Ne consegue una variazione sia nella velocità delle reazioni sia nei processi di trasporto. Poiché queste differenze vengono conservate in modo stabile nei processi di divisione cellulare, esse risultano fissate irreversibilmente alle cellule emergenti, determinandone le nuove caratteristiche. Il modello così descritto, anche se semplificato, rivela una dinamica evolutiva in grado di simulare il comportamento di colture cellulari reali. I risultati ottenuti presentano infatti una stretta corrispondenza con il comportamento osservato su colture batteriche, in particolare quelle di Escherichia coli.
È infine interessante osservare che il processo di diversificazione che emerge da tale analisi dinamica può essere applicato per descrivere non solamente la differenziazione cellulare, ma anche il comportamento di sistemi formati da unità in grado di replicarsi, quali la società umana e i sistemi ecologici.
Conclusioni
I sistemi chimici complessi manifestano una vasta tipologia di comportamenti che presentano spesso proprietà peculiari. La loro analisi costituisce una ricca fonte di modelli estremamente efficaci per esplorare nuovi territori riguardanti sia i sistemi naturali sia i processi produttivi nei quali la chimica gioca un ruolo di primo piano. Nei processi produttivi sono presenti reti di reazioni interconnesse la cui dinamica fa emergere situazioni talora imprevedibili. Alcuni esempi significativi sono stati illustrati in precedenza, con riferimento a situazioni molto diversificate, quali la preparazione di materiali, la formazione di strutture dendritiche cristalline e i processi morfogenetici che si manifestano nelle strutture organiche. Particolarmente ambiziose e affascinanti sono le ricerche intese a simulare il comportamento dei sistemi viventi. Alla loro base si devono fronteggiare due problemi fondamentali: (1) in che modo un insieme di molecole può dare origine alla varietà di comportamenti che caratterizzano le cellule; (2) in che modo le molecole possono assemblarsi in un insieme che abbia la capacità di dissipare l'energia, di autoreplicarsi e di adattarsi all'ambiente.
Allo stato attuale non è possibile stabilire se le conoscenze sulle caratteristiche delle molecole e delle loro interazioni ci potranno offrire una risposta a tali quesiti. Si tratta comunque di un programma che merita di essere perseguito. In ogni caso, è importante sottolineare che sulla base di alcuni aspetti peculiari dei sistemi presi in considerazione risulta possibile formulare interessanti modelli in grado di evidenziare l'emergere di comportamenti inaspettati di particolare interesse. Fra questi aspetti, abbiamo discusso la non linearità delle leggi cinetiche, la competizione fra le reazioni chimiche e la diffusione e i processi di retroazione, dimostrando che essi costituiscono efficaci strumenti per l'esplorazione di sistemi complessi soggetti a trasformazioni chimiche.
Bibliografia
Carrà, Morbidelli 1983: Carrà, Sergio - Morbidelli, Massimo, Chimica-fisica applicata, Milano, Hoepli, 1983.
Carrà 1989: Carrà, Sergio, La formazione delle strutture, Torino, Bollati Boringhieri, 1989.
Carrà 1998: Carrà, Sergio, Autorganizzazione, in: Enciclopedia del Novecento, Roma, Istituto della Enciclopedia Italiana, 1998, X, Suppl. II, pp. 75-99.
Eigen 1971: Eigen, Manfred, Self-organization of matter and evolution of biological macromolecules, "Naturwissenschaften", 58, 1971, pp. 465-523.
Endy, Brent 2001: Endy, Drew - Brent, Roger, Modelling cellular behaviour, "Nature", 409, 2001, pp. 391-395.
Kaneko, Yomo 1999: Kaneko, Kunihiko - Yomo, Tetsuya, Isologous diversification for robust development of cell society, "Journal of theoretical biology", 199, 1999, pp. 243-256.
Langer 1980: Langer, James S., Instabilities and pattern formation in crystal growth, "Reviews of modern physics", 52, 1980, pp. 1-28.
Masi 2001: Masi, Maurizio - Cavallotti, Carlo - Carrà, Sergio, Gas phase and surface kinetics of silicon chemical vapor deposition from silane and chlorosilanes, in: Silicon-based materials and devices, edited by Hari Singh Nalwa, San Diego-London, Academic Press, 2001, I, pp. 155-186.
Mazzotti, Carrà 1995: Mazzotti, Marco - Carrà, Sergio, Phase transition and symmetry-breaking in reacting chemical systems, in: Analysis, simulation, dynamics of chemical reactors, edited by Gaetano Continillo, Silvestro Crescitelli, Pier Giorgio Lignola, Napoli, CUEN, 1995, pp. 255-290.
Meinhardt 1992: Meinhardt, Hans, Pattern formation in biology: a comparison of models and experiments, "Reports on progress in physics", 55, 1992, pp. 797-849.
Newman, Comper 1990: Newman, Stuart A. - Comper, Wayne D., 'Generic' physical mechanisms of morphogenesis and pattern formation, "Development", 110, 1990, pp. 1-18.
Normile 1999: Normile, Dennis, Building working cells 'in silico', "Science", 284, 1999, pp. 80-81.
Peacocke 1983: Peacocke, Arthur R., An introduction to the physical chemistry of biological organizations, Oxford, Clarendon Press, 1983.
Service 1999: Service, Robert F., Exploring the systems of life, "Science", 284, 1999, pp. 80-83.
Solé, Goodwin 2000: Solé, Ricard - Goodwin, Brian, Signs of life, New York, Basic Books, 2000.
Tomita 2001: Tomita, Masaru, Whole-cell simulation: a grand challenge of the 21st Century, "Trends in biotechnology", 19, 2001, pp. 205-210.
Turing 1952: Turing, Alan M., The chemical basis of morphogenesis, "Philosophical Transactions of the Royal Society" (Series B), 237, 1952, pp. 37-72.
Whitesides, Ismagilov 1999: Whitesides, George M. - Ismagilov, Rustem F., Complexity in chemistry, "Science", 284, 1999, pp. 89-92.
Zewail 1996: Zewail, Ahmed H., Femtochemistry: recent progress in studies of dynamics and control of reactions and their transition states, "Journal of physical chemistry", 100, 1996, pp. 12701-12724.