IATROPATOLOGIA
Iatropatologia
Con il termine iatropatologia si intende l'insieme dei quadri morbosi causati, direttamente o indirettamente, dall'intervento del medico.
In questi ultimi decenni numerosi sono stati i progressi compiuti dalla medicina sia nel campo diagnostico sia in quello terapeutico, con conseguenti sostanziali benefici per lo stato di salute degli individui che di tale progresso hanno potuto beneficiare. Va comunque sottolineato che questo avanzamento tecnologico si è anche reso responsabile di numerosi effetti negativi a causa dei danni potenzialmente arrecabili all'organismo dalle nuove tecniche diagnostiche, terapeutiche, mediche o chirurgiche. L'impiego sempre più ampio di farmaci a scopo terapeutico e profilattico, la diffusione sempre più larga di presidi medico-chirurgici (per es., catetere, pacemaker, protesi artificiali) e di tecniche chirurgiche o mediche d'avanguardia (per es., interventi a cuore aperto, microchirurgia, trapianti d'organo, dialisi) vengono infatti pagati in termini di una nuova patologia, chiamata appunto iatropatologia.
Se può essere comprensibile che l'impiego delle nuove tecnologie possa comportare rischi e danni aggiuntivi, talora inevitabili, è altrettanto vero che gli effetti negativi sono accettabili solamente se i rischi che si corrono risultano inferiori ai benefici ottenibili e se non sono dovuti a un utilizzo improprio di tali tecnologie. Questi due presupposti, rapporto beneficio-rischio favorevole e utilizzo corretto delle tecnologie disponibili, devono essere sempre soddisfatti se non si vuole che l'inevitabile i. diventi colpevole danno.
Molto schematicamente possiamo perciò proporre una suddivisione della i. in base alle sue possibili cause, e precisamente: le tecniche diagnostiche invasive; gli interventi chirurgici; i farmaci.
Iatropatologia da tecniche diagnostiche invasive
La diffusione sempre più ampia di nuove tecniche diagnostiche invasive comporta inevitabilmente la comparsa e la diffusione di nuovi quadri iatropatologici, le cui caratteristiche cliniche sono analoghe a quelle riscontrabili in situazioni secondarie a cause diverse (per es., traumi, ferite).
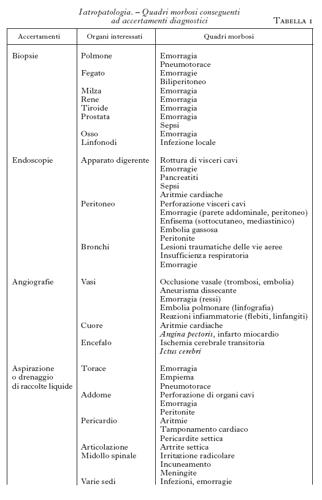
Nella tab. 1 viene riportata una lista delle complicanze più frequenti che possono verificarsi nel corso delle indagini diagnostiche invasive effettuate per le patologie più comuni. Come si può vedere, si tratta di situazioni morbose di varia natura a seconda dell'organo interessato e dell'accertamento invasivo eseguito. In tutte le situazioni è comunque chiamato in causa un meccanismo patogenetico simile, e cioè la perforazione, tramite ago o (meno frequentemente) tramite un catetere, di un organo, di un vaso o di una cavità. La lesione di continuo che ne segue può così causare direttamente un danno all'organo interessato o complicarsi con emorragie, infezioni o reazioni infiammatorie di maggiore o minore gravità. La rilevanza clinica e la frequenza di dette complicazioni dipendono da vari fattori, quali la difficoltà intrinseca della procedura o le condizioni cliniche del soggetto che si sottopone all'accertamento, ma importanza fondamentale riveste la capacità tecnica dell'operatore. Bisogna infatti ricordare che per ogni procedura esiste una curva di apprendimento che evidenzia come l'operatore più esperto sia anche colui che causa in genere minori complicazioni.
Iatropatologia da interventi chirurgici
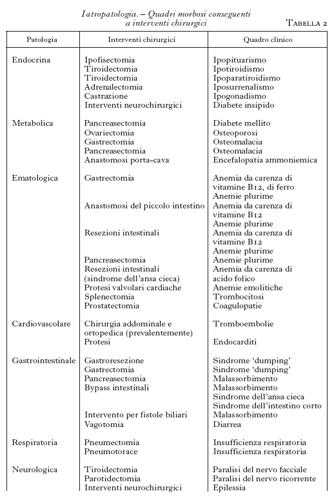
Le cause possibili sono di tre ordini: 1) la mutilazione di un organo, che può estendersi sino alla sua asportazione; 2) le complicanze perioperatorie; 3) le complicanze postoperatorie. Nella tab. 2 sono riassunti i quadri morbosi di più frequente riscontro.
Schematicamente si può affermare che i quadri iatropatologici sono espressione della perdita totale o parziale della funzione di uno o più organi o del trauma chirurgico di per sé.
Nel primo caso possono conseguire entità cliniche ben note e caratteristiche, elencate nella tab. 2. Nel secondo caso si tratta di complicanze aspecifiche, sintetizzabili in due entità morbose ben distinte, le complicanze emorragiche e quelle infettive, che possono manifestarsi durante o subito dopo l'intervento chirurgico (complicanze perioperatorie) o a distanza dallo stesso (postoperatorie). Molte delle considerazioni fatte per gli accertamenti invasivi possono essere replicate per gli interventi chirurgici. In particolare l'esperienza della équipe chirurgica e la possibilità di programmare l'intervento chirurgico (chirurgia elettiva) rispetto alla necessità di intervenire d'urgenza (chirurgia d'urgenza) rivestono una considerevole importanza nel ridurre il rischio iatrogeno. Da rilevare inoltre come le complicanze infettive e/o emorragiche richiedano per il loro trattamento farmaci e/o altri presidi terapeutici (per es., emotrasfusioni) a loro volta fonte di possibile danno iatrogeno (per es., epatiti virali, sepsi). Questo meccanismo (detto anche effetto domino) fa sì che i quadri morbosi conseguenti a un intervento invasivo possano essere molteplici e complessi.
Iatropatologia da farmaci
Sin da quando l'uomo ha cercato di utilizzare, sia pure in modo empirico, pratiche terapeutiche per curare i sintomi delle malattie più varie, è stata sempre viva la consapevolezza che gli interventi terapeutici possono essere fonte di danno, consapevolezza espressa dall'imperativo primum non nocere.
Con la continua introduzione di sempre nuovi farmaci, avvenuta a partire dagli anni Trenta, la storia della i. si è via via arricchita di episodi tragicamente significativi nel testimoniare come la tossicità dei farmaci richiedesse un'attenzione adeguata, che doveva interessare tutte le tappe del processo di produzione, commercializzazione e uso dei farmaci.
Per fare qualche esempio di tali episodi: negli Stati Uniti, nel 1906, la morte di diversi bambini a seguito dell'uso di un siero antidifterico contaminato con il bacillo del tetano; ancora negli Stati Uniti, nel 1930, la morte di almeno 100 persone a seguito dell'ingestione di uno sciroppo a base di sulfamidici in soluzione con glicole dietilenico; nel 1933 e nel 1950, rispettivamente, il riconoscimento che l'amidopirina e il cloramfenicolo potevano determinare discrasie ematiche letali; in Francia, nel 1954, la morte di più di 100 persone che avevano fatto uso di un composto organico a base di stagno; infine, nel 1961, il disastro della talidomide, che ha interessato tutto il mondo occidentale, Italia inclusa.
In quasi tutti i paesi, la pubblicazione delle farmacopee ufficiali e la definizione di tutta una serie di norme legislative volte a stabilire i criteri di fabbricazione, sperimentazione e commercializzazione dei farmaci hanno costituito i principali provvedimenti tesi a rispondere alle richieste di maggiore sicurezza nell'uso dei farmaci.
Quando si parla di danni iatrogeni connessi all'uso dei farmaci, si possono in ogni modo rilevare reazioni di tipo opposto: c'è chi sottolinea in termini drammatici la gravità del problema e chi invece tende a minimizzarlo. La ragione di questa disparità di giudizi risiede nella disomogeneità dei dati raccolti, a sua volta riconducibile a numerose cause: a) al diverso significato attribuito alla definizione di effetto indesiderato (EI) da parte di numerosi ricercatori; b) alla difficoltà di identificare con certezza un rapporto di causalità tra uso del farmaco e un certo effetto collaterale o tossico; c) al tipo particolare di casistica studiata; d) alle diversità metodologiche riscontrabili nella raccolta dei dati.
Per effetto indesiderato da parte di un farmaco si deve intendere un qualsiasi effetto che sia nocivo e non voluto e che si verifichi alle dosi in genere usate nell'uomo a scopo profilattico, diagnostico o terapeutico. Con questa definizione si escludono gli effetti legati all'abuso intenzionale di farmaci (a scopo di tossicomania o suicida), come pure gli insuccessi terapeutici che sono qualitativamente diversi dalle reazioni indesiderate vere e proprie.
Così definiti, i criteri per identificare e valutare un EI sembrano semplici e chiari, ma le difficoltà sorgono quando si tratta di dare loro pratica applicazione. La prima difficoltà risiede nell'aspecificità dei quadri clinici degli EI da farmaci, che possono essere indistinguibili da quelli dovuti a malattie varie non correlate all'uso di farmaci. Una seconda difficoltà è connessa all'identificazione delle reazioni, mentre la terza e fondamentale difficoltà risiede nel riuscire a stabilire un chiaro rapporto di causa ed effetto tra farmaco e reazione indesiderata osservata.
Questa difficoltà di giudizio è rispecchiata nella stessa classificazione degli EI adottata dai sistemi di registrazione ad hoc di alcuni paesi europei, che definisce una reazione indesiderata come certa quando non è spiegabile con le condizioni cliniche del paziente o con altre terapie non farmacologiche, quando l'evento segue alla somministrazione del farmaco con una sequenza temporale, quando la reazione presenta caratteristiche riconosciute come tipiche per quel farmaco, è migliorata o scomparsa con la sospensione del farmaco ma si è aggravata o è ricomparsa con la sua ripresa; come probabile, quando sono presenti le condizioni sopra menzionate salvo una (la dimostrazione della ricomparsa dell'EI alla ripresa del farmaco); come possibile, quando l'evento segue temporalmente in modo ragionevole alla somministrazione, esibendo caratteristiche tipiche della sostanza sospettata, ma potrebbe anche essere spiegato con lo stato clinico del paziente o attribuibile ad altri farmaci somministrati contemporaneamente; come incerta, quando l'evento segue temporalmente in modo ragionevole alla somministrazione ma non presenta caratteristiche riconosciute tipiche del farmaco incriminato, pur non potendo essere spiegato dallo stato clinico del paziente o dalla terapia concomitante (tutti i nuovi EI ricadono inizialmente in questa categoria); come non correlata, quando si verifica ogni altro evento che non risponde alle caratteristiche di cui sopra. L'adozione di queste definizioni allo scopo di standardizzare il processo logico di imputabilità è una condizione necessaria ma non sufficiente a garantire la piena riproducibilità, e il giudizio di correlazione rimane espresso in termini probabilistici, essendo l'affidabilità condizionata dalla qualità delle risposte, dalla quantità e completezza delle informazioni e dall'esperienza del medico.
Tutte queste incertezze nella definizione, nei giudizi di causalità, nella valutazione di merito e nelle metodologie, introducono elementi di disomogeneità che rendono i risultati dei diversi studi epidemiologici a nostra disposizione difficilmente interpretabili e comparabili.
Per quanto riguarda la morbilità, la variabilità dell'incidenza è notevole, andando da un minimo di 1,1% a un massimo del 35%, ed è imputabile ai motivi sopra esposti. I farmaci più incriminati sono gli antibiotici, alcuni cardiovascolari (digitale, chinidina, antipertensivi e diuretici), alcuni farmaci del sistema nervoso (ipnotici, sedativi, ansiolitici e antidepressivi), l'insulina e gli analgesici (acido acetilsalicilico). Ovviamente tale elenco risente del fatto che la maggior parte degli studi ha interessato malati acuti ricoverati in reparti medici, dove l'esposizione ai suddetti farmaci è prevalente.
Per ciò che riguarda i dati italiani, secondo uno studio prospettico pubblicato nel 1997 e condotto in un dipartimento d'emergenza di un grande ospedale, il 4,7% dei 5497 pazienti visitati in 3 mesi era affetto da condizioni patologiche correlate a farmaci e il 2,6% dei ricoveri era dovuto a una condizione iatropatologica. I farmaci più frequentemente incriminati sono risultati nell'ordine: gli antipertensivi, gli ipoglicemizzanti e altri farmaci cardiovascolari.
Gli studi che hanno preso in considerazione gli EI riconducibili a interazioni tra farmaci forniscono percentuali tra il 2% e il 7%. Se esaminiamo invece quanti ricoveri ospedalieri sono determinati da effetti tossici dovuti a farmaci ritroviamo dati meno discordi (4÷8% dei ricoveri), mentre non si hanno cifre sicure sull'entità del prolungamento della degenza che a essi sicuramente consegue. I dati sopra indicati riguardano reazioni indesiderate di grado moderato o severo (rispettivamente 60% e 40% di tutte le reazioni indesiderate da farmaci). È ovvio che, laddove non esista alcun sistema di rilevazione adeguato, gli EI connessi alle pratiche diagnostiche e terapeutiche vengono praticamente ignorati.
Per la mortalità, i dati sono forniti da pochi studi che stimano tali eventi attorno allo 0,1÷0,3% dei pazienti ricoverati in reparti medici. L'estrapolazione di questi tassi di mortalità al totale della popolazione ospedalizzata statunitense ha portato alcuni ricercatori a stimare in quel paese da 30.000 a 40.000 l'anno i morti per EI, con un costo per la sola degenza di 5 miliardi di dollari nel 1975.
L'industria farmaceutica, invece, contestando tali cifre, stima i decessi a non più di 2000÷3000 per anno, considerando solo gli EI che interessano i pazienti che non soffrono di affezioni di per sé letali. Più recentemente, estrapolando i dati disponibili presso il Registry of tissue reactions to drug dello Armed Forces Institute of Pathology e inserendo una serie di fattori correttivi che cercano di ovviare alle incertezze già segnalate, per gli USA è stato proposto di indicare il numero delle morti per i soli pazienti ospedalizzati in 5600÷11.500 l'anno. I farmaci più incriminati sono gli antiblastici, l'eparina, le soluzioni per via endovenosa, la digitale e i sali di potassio.
Metodologie più usate nella rilevazione degli effetti indesiderati
Sostanzialmente esse seguono due vie: la prima si basa sulla segnalazione spontanea da parte del medico degli EI riscontrati nella sua pratica quotidiana; la seconda sulla ricerca attiva degli EI a livello ospedaliero o ambulatoriale, utilizzando tecniche di ricerca diverse (caso-controllo, studi di coorte, studi ad hoc).
I sistemi di segnalazione spontanea da parte dei medici degli EI osservati sono presenti in diversi paesi, ma la loro efficacia si è dimostrata modesta. Infatti: a) solo una piccola parte delle reazioni indesiderate venute all'osservazione dei medici viene segnalata; b) le segnalazioni sono spesso incomplete e richiedono ulteriori indagini, non essendo spesso possibile stabilire se l'associazione tra EI e farmaco è accidentale o causale; c) non è possibile stabilire l'incidenza di un certo EI, non essendo calcolabile il numero delle persone che hanno assunto quel farmaco. D'altro lato i vantaggi di tale approccio metodologico sono ovvi: il sistema di sorveglianza interessa, perlomeno potenzialmente, tutti i pazienti che usano un determinato farmaco; il costo di gestione è contenuto e, soprattutto, i dati raccolti possono essere ulteriormente elaborati e approfonditi, possono cioè costituire il punto di partenza di ricerche ad hoc con una delle metodologie elencate nella tab. 3.
In realtà ogni metodo trova un'utilizzazione specifica a seconda del problema che si è chiamati ad affrontare. Il problema di una malattia indotta da farmaci è definito infatti dalla grandezza di due rischi: il rischio aggiuntivo di malattia indotta dal farmaco in chi lo usa e il rischio 'di base' esistente in assenza d'uso del farmaco. Ciascuno di questi due rischi può essere arbitrariamente definito come elevato, basso o intermedio a seconda dell'incidenza del fenomeno. In questo modo il tipo di approccio può essere determinato in base alla probabilità che i meccanismi di osservazione spontanea o la sperimentazione clinica prima dell'immissione del farmaco sul mercato non siano in grado di evidenziare il fenomeno, e in base alle possibilità che una certa malattia, in ogni categoria d'incidenza, possa essere correlata all'uso dei farmaci. La tab. 3 mostra appunto alcuni esempi di malattie indotte da farmaci, la metodologia che ha portato alla loro scoperta e l'approccio più corretto per affrontare problemi analoghi in futuro.
Basi farmacologiche degli effetti indesiderati
Gli effetti indotti da un farmaco sono il risultato di un'interazione tra la sostanza assunta, le caratteristiche del paziente e altri fattori (solo in parte conosciuti) in grado di modificare la risposta dell'organismo al medicamento. L'elenco dei fattori che possono modificare gli effetti di un farmaco comprende: la compliance, cioè il grado di adesione del paziente alla prescrizione del medico, che può comportare errori nella dose e/o nella modalità di somministrazione (per es., orari, rapporto temporale con il cibo o con altri farmaci); l'entità e la velocità di assorbimento del farmaco; il volume e la composizione in acqua e lipidi dell'organismo del paziente; la distribuzione del farmaco nei vari tessuti; il legame del farmaco alle proteine plasmatiche e tessutali; il tasso di eliminazione del farmaco; variabili fisiopatologiche, fattori genetici, interazioni con altri farmaci, fattori tutti in grado di modificare la concentrazione del farmaco nella sede di azione; il tipo di interazione farmaco-recettore, lo sviluppo di tolleranza, l'effetto placebo, fattori questi in grado di influenzare l'intensità dell'effetto.
Questa interazione interessa sia gli effetti terapeutici che quelli indesiderati e permette di comprendere perché i meccanismi con cui si realizzano gli EI siano così complessi e ancora poco conosciuti. È possibile comunque cercare di spiegare perché alcuni individui a differenza di altri presentino una reazione indesiderata a un certo farmaco, in base alle differenze quantitative o qualitative, di ordine farmacodinamico (cioè dovute all'interazione tra il farmaco e i siti nei quali esso esercita la sua azione nei vari organi o tessuti) o farmacocinetico (vale a dire, dovute a variabilità nei livelli di assorbimento, distribuzione nell'organismo, metabolismo ed eliminazione del farmaco), esistenti tra i diversi individui.
In base alla patogenesi, cioè al meccanismo con cui si realizzano, gli EI vengono distinti in EI di tipo A ed EI di tipo B.
Gli EI di tipo A derivano da un'esagerata risposta alla normale azione farmacologica, spesso multipla, del medicamento, a sua volta riconducibile a modificazioni quantitative di tipo farmacocinetico o di tipo farmacodinamico. Gli EI di tipo A sono in genere prevedibili in quanto già conosciuti e quindi almeno teoricamente prevenibili, sono dose-dipendenti e si presentano con frequenza piuttosto elevata, ma raramente costituiscono una minaccia per la vita del paziente.
Gli EI di tipo B derivano da una risposta qualitativamente aberrante da parte dell'organismo, risposta che dev'essere fatta risalire a differenze qualitative di tipo farmacocinetico e/o farmacodinamico. Gli EI di tipo B non sono prevedibili e quindi prevenibili, non sono dose-dipendenti e, anche se rari, sono di solito gravi e spesso fatali. L'abnorme risposta del paziente alla somministrazione del farmaco può verificarsi per l'esistenza di una predisposizione genetica in senso lato o a causa di fenomeni immunologici.
A conclusione di quanto sinora detto a proposito dell'eziopatogenesi degli EI va ancora ribadito che la classificazione da noi adottata non è onnicomprensiva. In essa sono difficilmente inquadrabili reazioni anche importanti, quali, per es., fenomeni particolari come la modificazione della flora microbica in rapporto all'uso di antibiotici. Inoltre esistono situazioni in cui i vari meccanismi patogenetici degli EI sono contemporaneamente presenti e si potenziano reciprocamente. Il caso paradigmatico è quello dei pazienti affetti dal virus HIV, specialmente se in fase di malattia AIDS. Questi pazienti sono predisposti agli EI da farmaci, in particolare antivirali e farmaci utilizzati per prevenire o curare le infezioni opportunistiche. I fattori di principale importanza nel condizionare tale elevata incidenza di EI sono due: la tossicità intrinseca dei farmaci usati, in particolare gli antivirali, e l'aumentata probabilità di reazioni immunomediate come risultato della perdita della normale regolazione dell'attività dei linfociti B, conseguente alla distruzione dei linfociti T-helper. Tre fattori potenziano ulteriormente gli effetti della tossicità e della disregolazione immunitaria: la lunga durata dei trattamenti, l'elevato numero di farmaci necessari a questi pazienti (con conseguente rischio di interazioni), l'ipotizzata minore capacità di metabolizzazione dei farmaci da parte dei pazienti con AIDS.
Fattori predisponenti all'insorgenza degli effetti indesiderati
Numerosi sono i fattori in grado di facilitare la comparsa di EI tramite uno o più dei meccanismi eziopatogenetici sopra considerati. Quelli ritenuti più importanti meritano una trattazione specifica, data la loro rilevanza pratica al fine della prevenzione e del controllo.
Caratteristiche del farmaco
I farmaci dotati di molteplici azioni farmacologiche e di un indice terapeutico (cioè la differenza fra dose terapeutica e dose tossica) basso, somministrati a dosi elevate, per lunghi periodi di tempo e per via parenterale, sono quelli che più facilmente creano problemi. Le ragioni sono ovvie: la molteplicità degli effetti fa sì che accanto a quello voluto si manifestino contemporaneamente uno o più degli effetti non correlati allo scopo terapeutico e quindi indesiderati.
La vicinanza tra dose terapeutica e dose tossica, associata alla grande variabilità individuale di risposta, facilita per numerosi farmaci la comparsa di fenomeni tossici altrimenti evitabili (per es., la digitale, l'aminofillina, la nortriptilina ecc.). Così pure la necessità di somministrare un farmaco a dosi elevate e per lunghi periodi di tempo fa sì che rischi altrimenti marginali si manifestino in tutta la loro evidenza (per es., il caso dei corticosteroidi, dei contraccettivi orali e dei β-bloccanti). Si aggiunga che la stessa via di somministrazione può essere rilevante, in quanto la somministrazione parenterale, per es., permette a una grande quantità di farmaco di trovare accesso direttamente al circolo e facilita così l'insorgenza di certi EI o ne aggrava l'intensità (per es., gli effetti correlati all'uso delle soluzioni elettrolitiche endovenose, del glicerolo ecc.).
Caratteristiche del paziente. Tra le diverse variabili, le più importanti sono quelle rappresentate dall'età, dal sesso, dalla presenza di una gravidanza o di malattie in grado di modificare la risposta dell'organismo ai farmaci somministrati.
Per quanto riguarda l'età, i dati epidemiologici evidenziano come gli EI siano più frequenti nei bambini e nei vecchi; ciò è da attribuirsi a numerosi fattori concomitanti, quali la presenza di patologie spesso multiple, di una politerapia, di una scarsa compliance, nonché di differenze di ordine farmacocinetico e farmacodinamico esistenti in queste fasce estreme di età, che vanno perciò considerate a rischio per gli EI e nelle quali l'uso dei farmaci va quindi attuato con prudenza e massima attenzione a un loro corretto impiego.
Il sesso è sicuramente meno importante, ma alcune diversità tra i due sessi comunque esistono: per es., le donne sono più soggette alla nausea e al vomito da chemioterapia antitumorale.
La gravidanza pone dei problemi del tutto particolari. La gestazione sembra infatti alterare la risposta dell'organismo a taluni farmaci per motivi in parte comprensibili (espansione del volume plasmatico, modificazioni ormonali) e in parte meno ovvi (forse, alterata sensibilità dei recettori: per es., la sensibilità del fegato all'effetto epatotossico della tetraciclina sembra aumentata). Ma il vero problema è costituito dalla presenza del feto e dalle caratteristiche della barriera placentare. La placenta infatti non costituisce un ostacolo al trasferimento dei farmaci, e questo accentua i rischi di comparsa di EI a carico del feto. Quest'ultimo presenta alcune peculiarità anatomofunzionali che possono favorire l'effetto tossico dei farmaci, quali: una maggiore permeabilità della barriera ematoliquorale, un'immaturità enzimatica a livello di più organi, un aumento del compartimento liquido extracellulare, un diminuito tasso di proteine plasmatiche, un'immaturità dei recettori d'organo e, soprattutto, uno stato di delicata differenziazione tessutale (specie nei primi mesi di gravidanza). Va comunque tenuto presente che, durante la gestazione, un farmaco in genere non si accumula nel feto in quanto alla sua escrezione provvede l'apparato emuntore materno. Al momento del parto però la situazione muta radicalmente e il neonato si trova costretto a provvedervi autonomamente. L'eliminazione del farmaco è tuttavia compromessa dalla scarsa efficienza dei suoi meccanismi di escrezione.
Da quanto detto consegue l'imperativo di utilizzare farmaci in gravidanza soltanto se essi sono assolutamente indispensabili e solo dopo aver consultato il medico. I rischi iatrogeni da farmaci per il feto sono infatti spesso quantificabili soltanto in modo approssimativo. Una situazione parzialmente sovrapponibile si ha anche durante l'allattamento.
Malattie associate o intercorrenti
Talora lo stato di malattia è in grado di aumentare la suscettibilità del paziente al manifestarsi degli EI, in quanto è capace di indurre modificazioni di ordine farmacocinetico o farmacodinamico. Particolarmente rilevanti sono le malattie che compromettono la funzione di organi come il fegato o il rene, e in tal modo riducono la loro capacità di metabolizzare o di eliminare dall'organismo i farmaci con conseguente loro accumulo e tossicità.
Fattori addizionali. Tra i fattori esterni che possono predisporre alla comparsa di alcuni EI sono da ricordare: la malnutrizione, il fumo, l'ingestione di alcool e numerosi farmaci.
La malnutrizione può facilitare la comparsa di alcuni EI, per le modificazioni che è in grado di indurre a carico del quadro sieroproteico. L'ipoalbuminemia a essa conseguente può infatti, per le ragioni già accennate, alterare la cinetica di alcuni farmaci e permettere il raggiungimento di elevati tassi ematici di farmaco attivo (libero).
Il fumo di sigaretta può costituire un rischio aggiuntivo nell'uso di certi farmaci assunti cronicamente, a causa della possibile induzione di alcuni enzimi microsomiali e della conseguente modificazione del metabolismo di alcune sostanze. È il caso dell'aminofillina, i cui livelli ematici possono elevarsi sino a provocare fenomeni tossici a seguito dell'interruzione del fumo e della conseguente minore metabolizzazione epatica.
L'alcool può predisporre all'insorgenza di EI inibendo o inducendo i sistemi enzimatici microsomiali epatici e quindi riducendo o incrementando rispettivamente il metabolismo dei farmaci. L'assunzione acuta in genere inibisce tali sistemi enzimatici e quindi riduce il metabolismo dei farmaci assunti (per es., doxiciclina, pentobarbital, tolbutamide, amitriptilina, sedativi), potenziandone di conseguenza l'effetto, mentre l'assunzione cronica, tramite l'induzione dei sistemi enzimatici, ne accelera il metabolismo e ne riduce l'effetto. Inoltre l'alcool può presentare interazioni farmacodinamiche con numerosi farmaci; per es., effetti di sommazione dell'effetto farmacologico si verificano con benzodiazepine e antidepressivi triciclici (maggiore sedazione), ipoglicemizzanti orali (ipoglicemia grave e prolungata), anticoagulanti orali e antinfiammatori non steroidei (maggior rischio di sanguinamento). Infine alcuni farmaci inibiscono il metabolismo dell'alcool con accumulo di acetaldeide e conseguenti EI (per es., nausea, vomito, flush cutaneo, cefalea, ipotensione con metronidazolo e alcune cefalosporine di 2ª e 3ª generazione).
L'uso concomitante di altri farmaci costituisce sicuramente un ulteriore importante fattore predisponente all'insorgenza di EI. Non sempre però un'interazione dev'essere considerata un evento pericoloso o clinicamente significativo. Sono i farmaci a basso indice terapeutico (rientrano fra questi, per es., gli anticoagulanti, gli ipoglicemizzanti orali, gli antiblastici, gli anticonvulsivanti, i triciclici), d'impiego molto frequente e spesso usati in combinazione per il trattamento di specifici quadri morbosi, quelli che assumono un'importanza pratica rilevante.
Va infine sottolineato che gli EI conseguenti a un'interazione si possono manifestare sia nel corso del trattamento concomitante sia al momento della sospensione di uno dei farmaci, come nel caso di meccanismi che tendono a ridurre la quantità di farmaco attivo o sospendono il controllo di alcuni effetti collaterali. Al fine della prevenzione di queste reazioni va tenuta presente pertanto la necessità di sorvegliare il paziente sia al momento della somministrazione sia al momento della sospensione di un farmaco.
Quadri clinici delle malattie iatrogene
I quadri clinici iatrogeni indotti dai farmaci (a quelli conseguenti alle procedure diagnostiche e agli interventi chirurgici si è accennato in precedenza) sono sovrapponibili a quelli dovuti ad altri agenti causali, e interessano praticamente tutti i tessuti, apparati e funzioni dell'organismo, in modo singolo o combinato. Non esistono cioè quadri clinici caratteristici che ci consentano di identificare subito il danno come iatrogeno.
Questo fatto, oltre a rendere difficile il riconoscimento del rapporto causale tra fenomeno morboso osservato nel singolo paziente e somministrazione del farmaco, fa anche sì che sia praticamente impossibile elencare tutte le numerose manifestazioni cliniche attribuibili ai farmaci in commercio. Va solo sottolineato come alcuni di questi quadri si presentino più comunemente con certi farmaci e in determinati pazienti.
A tale esemplificazione aggiungiamo la trattazione molto schematica di alcuni EI particolarmente gravi legati a farmaci di diffusissimo impiego, per sottolineare ancora una volta l'estrema importanza che riveste per il medico pratico la conoscenza precisa dei rischi potenziali di un trattamento farmacoterapico.
Penicilline. - I farmaci appartenenti a questo gruppo terapeutico vengono citati a esempio per il loro indice terapeutico estremamente favorevole, sia a lungo che a breve termine. Eppure anche le penicilline possono essere responsabili di gravi, anche se rare, reazioni allergiche. Queste ultime possono essere di due tipi: 1) una reazione immediata, spesso letale, caratterizzata da shock, edema della glottide e sincope; 2) una reazione ritardata con una sintomatologia simile alla malattia da siero, caratterizzata da rash, orticaria, febbre, tumefazioni e dolori poliarticolari.
Un test cutaneo positivo non implica con certezza che il paziente svilupperà una reazione allergica, ma soltanto che quest'ultima si può presentare con frequenza elevata (20÷30% dei soggetti cuti positivi). D'altra parte un test negativo non garantisce una totale sicurezza di impiego delle dosi terapeutiche. Fondamentali perciò rimangono le precauzioni d'uso per trattare un eventuale shock anafilattico (non prevenibile con la somministrazione di antistaminici o di corticosteroidi), e cioè la disponibilità di adrenalina e del necessario per una intubazione e rianimazione del paziente.
Farmaci antinfiammatori non steroidei (FANS). - Vengono compresi in tale categoria i salicilati (il cui prototipo è l'aspirina) e altri antinfiammatori chimicamente non correlati all'aspirina. I FANS sono tra i farmaci più frequentemente utilizzati per le loro proprietà antinfiammatorie, antipiretiche, analgesiche e antitrombotiche, che li rendono molto utili per il trattamento o la prevenzione di un grande numero di condizioni patologiche.
Proprio per la loro diffusa utilizzazione possono essere di frequente responsabili di EI, principalmente a carico dell'apparato gastroenterico e renale (fig. 3). Il meccanismo con cui si realizza il danno a carico gastroenterico non è del tutto ben conosciuto, ma coinvolge un'azione sia locale che sistemica e quindi il danno può verificarsi anche dopo assunzione per via parenterale o rettale. I disturbi variano da turbe digestive banali (nausea, bruciore, difficoltà digestive) a manifestazioni potenzialmente gravi come emorragie e ulcerazioni. Le categorie di pazienti più a rischio sono gli anziani, specie le donne, e i pazienti con storia di ulcera peptica o con ulcera peptica in atto. Per quanto riguarda il danno renale, caratterizzato dall'instaurarsi di un'insufficienza renale, esso si verifica più frequentemente in pazienti con preesistente compromissione della funzione renale, negli anziani in genere e in caso di uso concomitante di altri farmaci nefrotossici.
Diuretici. - La diffusione e la gravità della patologia alla quale si indirizzano ne giustificano l'ampio uso, anche se ciò ha indubbiamente aumentato il numero degli EI a essi attribuibili. Gli EI più frequenti e preoccupanti riguardano l'equilibrio idroelettrolitico e sono rappresentati dall'ipokaliemia (ma anche dall'iperkaliemia), dall'ipomagnesiemia, dall'iposodiemia, dall'ipocloremia e dall'alcalosi. L'età avanzata, l'uso contemporaneo di altri farmaci cardiovascolari (digitale, antiaritmici), la potenza del diuretico impiegato, i trattamenti a dosi elevate e protratti nel tempo, sono fattori di rischio aggiuntivi che, se non tenuti in considerazione, possono condurre alla comparsa di quadri sintomatologici anche gravi, quali alcalosi ipocloremica, aritmie cardiache, miolisi ipokaliemica, coma epatico, iperazotemia prerenale, iponatriemia diluizionale, ipotensione e disidratazione.
Antipertensivi
Potrebbero ripetersi per questa categoria le considerazioni fatte a proposito dei diuretici. Appare utile sottolineare come l'avanzare delle conoscenze del settore e le nuove scoperte della ricerca farmaceutica forniscano al medico prodotti sempre nuovi e più efficaci. Questo fatto, se permette al medico di trattare in modo soddisfacente forme di ipertensione una volta difficilmente controllabili, lo obbliga al contempo a uno sforzo di attenzione costante per poter rilevare e prevenire gli EI dei nuovi farmaci. Basterà citare le crisi ipertensive (anche letali) da sospensione brusca della clonidina, le crisi sincopali connesse all'inizio della terapia con prazosin, gli infarti del miocardio conseguenti all'improvvisa interruzione dell'assunzione dei β-bloccanti e infine l'insufficienza renale da captopril. Gli EI più gravi sono quelli connessi a un eccessivo abbassamento della pressione arteriosa a causa di un trattamento con farmaci o con dosi inappropriate. Si possono così verificare paradossalmente episodi morbosi simili a quelli che il trattamento dell'ipertensione tende a prevenire, e cioè episodi di ischemia cerebrale transitoria, ictus cerebrale e infarto del miocardio.
Psicofarmaci
Sotto questa denominazione possono essere comprese almeno tre categorie di farmaci: gli ansiolitici, gli antidepressivi e gli antipsicotici.
Tra gli ansiolitici le benzodiazepine sono sicuramente i farmaci più utilizzati, e di cui si fa il maggiore abuso, perché vengono considerate prive di EI rilevanti. Ciò, se è vero per un uso a breve termine e in dosi ridotte, non lo è per un uso protratto e a dosi elevate. In quest'ultimo caso infatti le benzodiazepine sono in grado di indurre dipendenza fisica e psichica alla stessa stregua dei barbiturici.
Per gli antipsicotici la situazione è ancora più seria in quanto questi farmaci sono in grado di indurre EI gravi sia nel corso di brevi cicli terapeutici (dalle reazioni extrapiramidali alle epatiti colostatiche, dalle agranulocitosi alle dermatiti esfoliative), sia a seguito del loro uso protratto nel tempo (dalla ginecomastia e impotenza alle aritmie cardiache). In quest'ultimo caso, particolarmente grave è il quadro morboso della discinesia tardiva, affezione invalidante e irreversibile, sconosciuta prima che venisse impiegata questa categoria di farmaci. Analoga si presenta la situazione per quanto riguarda gli antidepressivi.
Appare ovvio di fronte a questi gravi EI suggerire la massima cautela nell'uso di tali farmaci. Non solo: la loro utilizzazione terapeutica richiede anche una notevole esperienza clinica per la necessità di conoscenze specifiche, di una precisione diagnostica e di una concomitante utilizzazione di un'adeguata psicoterapia. Quanto detto suggerisce la necessità di affidare la prescrizione di questi farmaci (o almeno di alcuni di essi) soltanto al medico specialista.
Mezzi di contrasto iodati
L'estendersi delle pratiche diagnostiche che si avvalgono di mezzi di contrasto iodati (angiografie, urografie, broncografie ecc.) ha posto in primo piano il problema degli EI che tali composti sono in grado di provocare. Essi possono essere classificati in tre categorie: 1) EI causati da somministrazione di una dose massiva di mezzo di contrasto (come, per es., nell'angiocardiogramma); 2) EI conseguenti alla concentrazione elevata del mezzo di contrasto in un particolare organo (come, per es., l'urografia); 3) EI correlati a reazioni allergiche.
Mentre le due prime categorie di EI, che si manifestano con una patologia d'organo specifica, possono essere previste e in parte prevenute, l'ultimo gruppo è particolarmente grave nelle sue estrinsecazioni cliniche ed è imprevedibile. Lo spettro clinico di queste reazioni allergiche è assai ampio, andando dall'anafilassi, spesso letale, alla semplice eruzione orticarioide, dall'arresto cardiaco sino all'edema angioneurotico. Fortunatamente l'incidenza delle reazioni è piuttosto bassa e variabile a seconda dei mezzi di contrasto utilizzati.
Per es., secondo un recente report dell'agenzia statunitense Food and drug administration (Lasser, Lyon, Berry 1997), i mezzi di contrasto a elevata osmolarità sono gravati da un maggior numero di reazioni avverse, di reazioni avverse gravi e di morti, se comparate con i mezzi di contrasto non ionici e a bassa osmolarità (incidenza per milione di esami svolti: reazioni avverse 193,8 contro 44,4; reazioni avverse gravi 37,4 contro 10,5; morti 3,9 contro 2,1). Peraltro l'incidenza di casi di insufficienza renale era circa 3,6 volte più elevata con i mezzi di contrasto a bassa osmolarità che con i mezzi di contrasto a osmolarità elevata.
Nel determinare il tipo e la gravità della reazione entrano ovviamente in gioco numerosi fattori condizionanti l'insorgenza di reazioni allergiche, già citati. Anche se non esiste alcun mezzo sicuro per prevenire l'insorgenza di tali EI, va comunque sottolineato che là dove si rispettino le controindicazioni usuali all'esecuzione di tali accertamenti e là dove si mettano in atto tutte le precauzioni necessarie per trattare immediatamente le reazioni che si dovessero presentare, l'uso dei mezzi di contrasto iodato è da ritenere generalmente sicuro.
Prevenzione e controllo degli effetti indesiderati
Da quanto esposto risulta chiaro che non tutti gli EI sono prevedibili o controllabili. All'atto pratico, tuttavia, una parte probabilmente rilevante delle manifestazioni iatropatologiche da farmaci potrebbe essere evitata tenendo presenti alcuni principi fondamentali qui di seguito elencati:
1) il rischio di un EI è un'inevitabile conseguenza dell'uso di farmaci efficaci, e quindi dovrebbe essere sempre tenuto presente al momento della prescrizione; 2) il rischio di una comparsa di EI deve essere sempre minore rispetto al possibile beneficio derivabile dal trattamento; 3) è essenziale conoscere perfettamente le caratteristiche del farmaco impiegato, per poter valutare correttamente il rapporto rischio-beneficio o per poter mettere in atto tutte le precauzioni necessarie onde evitare o ridurre i rischi potenziali; 4) vanno attentamente considerate le caratteristiche fisiopatologiche del paziente in grado di modificare l'usuale risposta dell'organismo al farmaco; 5) il rischio di EI aumenta con il crescere del numero dei farmaci prescritti; il loro numero va perciò contenuto; 6) i medici devono fornire al paziente un'informazione sufficiente sulle reazioni indesiderate più frequenti, sulle interazioni e sulle corrette modalità di assunzione del farmaco prescritto, e verificare per quanto possibile che il paziente abbia ben compreso e accetti o meno il farmaco; 7) gli effetti delle reazioni non prevedibili (allergia, anafilassi) possono essere contenuti nella loro gravità con semplici precauzioni prima dell'inizio o nel corso della terapia; 8) in presenza di un quadro clinico difficilmente descrivibile, che interessa un paziente in trattamento con farmaci, va presa in seria considerazione l'ipotesi di un quadro morboso indotto dalla terapia; questa andrà perciò sospesa e il malato attentamente sorvegliato; 9) è compito del medico riconoscere la presenza di un EI, segnalarlo secondo le modalità previste dalla legge ed educare il paziente sul modo di prevenire gli EI già noti; 10) è compito del paziente informare il medico di ogni fatto nuovo rilevante che si manifesti nel corso di una terapia, specie se da poco iniziata o modificata, nonché seguire con attenzione i consigli del medico in merito alle modalità di impiego del farmaco, informandolo di ogni variazione eventualmente occorsa.
In conclusione si può perciò affermare che, anche se l'entità della patologia da farmaci è difficilmente quantificabile, e senza voler mettere in discussione i benefici procurati dai moderni presidi terapeutici farmacologici, quando essi siano efficaci, razionali e impiegati in modo appropriato, il quadro epidemiologico degli EI e soprattutto il modo con il quale l'uso dei farmaci si espande, spesso in modo ingiustificato e irrazionale, impongono al medico (ma anche al farmacista, all'industria farmaceutica, all'autorità di controllo e agli stessi pazienti) un serio ripensamento sulla portata del problema. Ripensamento che deve tramutarsi in atteggiamenti concreti volti a correggere le distorsioni esistenti a livello della prescrizione (ma anche della produzione, delle procedure di immissione in commercio, del controllo e dell'informazione sui farmaci) perché possa compiutamente realizzarsi l'imperativo primum non nocere.
bibliografia
L.S. Goodman, A. Gilman, The pharmacological basis of therapeutics, New York 1941, 1975⁵.
H. Jick, The discovery of drug induced illness, in New England journal of medicine, 1977, 296, pp. 481-85.
G. Casadei, A. Silva, Farmacosorveglianza, Milano 1989.
A. Del Favero, Malattie iatrogene, in P. Larizza, D. Furbetta, Compendio di medicina interna e terapia, Padova 1993, pp. 2581-608.
Side effects of drugs annual, 1996, pp. 1-502.
E.C. Lasser, S.G. Lyon, C.C. Berry, Reports on contrast media reactions: analysis of data from reports to the U.S. Food and drug administration, in Radiology, 1997, 203, pp. 605-10.
F. Raschetti, I. Menniti, M. Morgutti et al., Adverse drug events in hospitalized patients, in The journal of the American medical association, 1997, 277, pp. 351-54.
J.P. Utrecht, Current trends in drug-induced autoimmunity, in Toxicology, 1997, 119, pp. 37-43.