FECONDAZIONE
Fecondazione
(XIV, p. 927; App. II, i, p. 909; v. anche bioetica, App. V, i, p. 368)
Fecondazione artificiale e assistita
La possibilità di assistere, in vario modo, le coppie sterili o scarsamente fertili desiderose di prole è stata presa in considerazione dai medici per molto tempo, con risultati del tutto inconsistenti, soprattutto a causa delle scarse conoscenze acquisite sulla fisiopatologia della riproduzione umana.
Il problema della sterilità
Il problema della sterilità degli individui e delle coppie è stato a lungo considerato di modesto rilievo clinico e sociale e solo recentemente la medicina ha iniziato a occuparsene con impegno. Questa maggior attenzione è dovuta sia al fatto che la richiesta di intervento da parte delle coppie sterili è divenuta progressivamente più pressante, sia alla maggior frequenza della sterilità tra le coppie che desiderano avere figli. Le ragioni dell'aumento della sterilità non sono del tutto chiare: si tratta probabilmente di numerosi fattori, non tutti facili da quantificare, tra i quali certamente prevalgono il progressivo inquinamento ambientale, i mutamenti dell'igiene di vita e dei comportamenti individuali e la scelta di avere figli in età progressivamente più avanzata. Ne deriva che, nei paesi occidentali, più del 15% delle coppie che desiderano avere un figlio devono ricorrere alle cure dei medici specialisti; una percentuale che sembra aumentare continuamente e che comprende al proprio interno cause maschili e femminili in numero quasi identico.
Le inseminazioni e le banche del seme
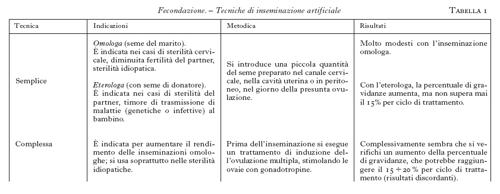
La storia delle f. artificiali più semplici (tab. 1), quelle nelle quali il medico si limita a inserire il seme nella vagina o nell'utero della donna, ha un inizio piuttosto recente. A raccomandare per la prima volta l'uso dell'inseminazione omologa (cioè eseguita con il seme del marito) fu W. Hunter nel 1780 e i primi risultati relativi a casi di impotenza coeundi furono riportati da un medico francese, J.G. Thouret, nel 1803. Le prime inseminazioni con seme di donatore (cioè eterologhe) risalgono alla fine dell'Ottocento, ma bisogna arrivare al 1953, anno in cui R.Ph. Shearman annunciò i successi conseguiti con seme congelato, per registrare alcuni risultati concreti e l'istituzione delle prime banche del seme, che garantivano la mancanza di rapporti tra chi dona e chi riceve, la disponibilità di campioni di seme con differenti caratteristiche (aspetto fisico, per es., e gruppo sanguigno) e la possibilità di eseguire controlli adeguati per evitare la trasmissione di malattie sessuali.
Attualmente, le banche del seme per inseminazione eterologa (nate anche per conservare il seme di persone che devono essere sottoposte a trattamenti sterilizzanti) sono diffuse in gran parte del mondo occidentale, sebbene con norme e regolamenti molto diversi.
Le principali linee guida, condivise in pratica dovunque, riguardano la selezione dei donatori, che non deve essere rivolta a identificare individui con particolari caratteristiche positive (del resto, quasi mai trasferibili nella progenie), ma piuttosto a selezionare persone sane e nelle cui famiglie non siano presenti malattie genetiche di rilievo. Le banche del seme sono anche generalmente impegnate a non utilizzare il seme di un donatore dopo che con lo stesso seme sono nati più di un certo numero di bambini (da 3 a 9) in differenti famiglie. È poi responsabilità delle banche del seme evitare di utilizzare seme infetto: per questa ragione, il liquido seminale viene congelato e utilizzato solo dopo un lungo periodo di tempo, necessario per controllare, nel donatore, la persistenza della negatività sierologica nei confronti delle principali malattie infettive note.
Le fecondazioni assistite
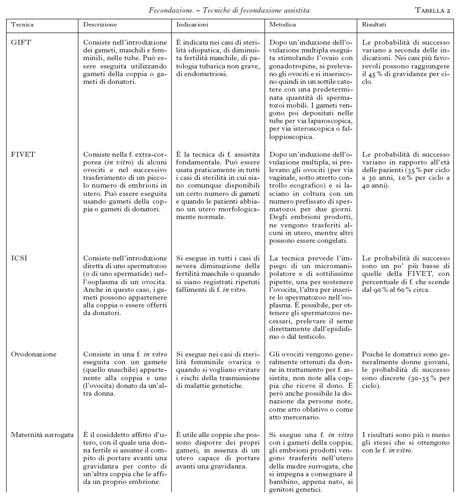
Per capire la storia delle f. medicalmente assistite (tab. 2), cioè di quelle tecniche che prevedono una manipolazione dei gameti (spermatozoi e ovociti), è necessario tener conto di due elementi: da una parte le conquiste ottenute in questo campo dalla medicina veterinaria e dalla biologia sperimentale (il primo tentativo di f. in vitro con gameti di mammiferi risale al 1878); dall'altra la considerazione attenta dei mutamenti avvenuti nelle organizzazioni familiari e nel significato e nel valore che i bambini hanno nel loro contesto e, insieme, del diffondersi della sterilità di coppia, che assume progressivamente il senso di un profondo malessere sociale (si parla, per l'Europa, di percentuali di sterilità di coppia comprese tra il 15 e il 20%).
La fecondazione in vitro: la FIVET. - Il tentativo di fecondare un ovocita umano in vitro (cioè in un terreno di coltura, fuori dal corpo materno) fu praticato per la prima volta a Melbourne nel 1973. Il primo vero successo risale, però, soltanto al luglio del 1978, quando in Inghilterra avvenne la nascita di Louise Brown, dopo un procedimento di f. in vitro eseguito da R. Edwards e P. Steptoe. L'idea originale era quella di risolvere il problema della sterilità tubarica non suscettibile di correzione chirurgica, una delle cause più frequenti di sterilità coniugale. Molto rapidamente, però, l'indicazione si è allargata ai casi di sterilità da cause non conosciute, di scarsa fertilità maschile, di sterilità da cause immunologiche.
Questa tecnica (FIVET: Fertilization In Vitro Embryo Transfer) prevede nell'ordine: una terapia di stimolo ovarico, eseguita generalmente con l'impiego di gonadotropine ipofisarie, che ha l'intento di far maturare contemporaneamente numerosi follicoli ovarici; il prelievo, in analgesia o in anestesia, degli ovociti contenuti in questi follicoli; la loro incubazione, in un terreno di coltura adatto, insieme al seme del marito o del compagno; il trasferimento in utero - con una manovra non traumatica - degli embrioni ottenuti.
Dal momento che queste tecniche sono caratterizzate da una bassa percentuale di successi (non più del 15÷20% in media per ciclo di trattamento, con notevoli variazioni a seconda dell'età delle donne trattate), si è cercato di migliorare i risultati trasferendo più di un embrione, ma sempre tentando di evitare di ottenere gravidanze multiple, poiché l'impianto di molti embrioni rappresenta un grave problema ostetrico e un ancor più grave problema di medicina neonatale.
Le gravidanze multiple. - La percentuale di gravidanze multiple nelle f. assistite è molto elevata, poiché raggiunge - e in alcune casistiche supera - il 20%. È da tenere presente che si tratta generalmente di gravidanze gemellari e che l'attuale tendenza a trasferire due embrioni nelle donne più giovani e tre o quattro nelle donne meno giovani ha ridotto il numero dei casi più drammatici, nei quali si impiantavano contemporaneamente in utero fino a dieci embrioni. Malgrado questi dati, gravidanze trigemine e quadrigemine continuano, anche se più raramente, a verificarsi e l'uso di tecniche empiriche quali le induzioni dell'ovulazione multipla nelle sterilità inspiegate continua a presentare sorprese molto sgradevoli. I problemi posti da queste gravidanze sono molteplici: da un lato, esse facilitano la comparsa della sindrome da iperstimolazione ovarica (v. oltre) e di molte delle più temibili complicazioni ostetriche (gestosi, ipertensione, diabete); dall'altro, sono frequentemente responsabili di aborto e di parto prematuro, con nascita di bambini particolarmente piccoli e la cui sopravvivenza - tra l'altro spesso minata da deficit neurologici - è connessa con la possibilità di nascere in ambienti medici particolarmente attrezzati, dove esistono centri di assistenza intensiva neonatale. Nelle cosiddette grandi gravidanze multiple, quando sia evidente l'impossibilità di portare avanti la gravidanza stessa a causa del numero dei feti presenti in utero, viene utilizzata una tecnica di aborto selettivo (embrioriduzione), consistente nell'eseguire iniezioni mortali, sotto controllo ecografico, a una parte degli embrioni, cercando così di garantire la sopravvivenza di quelli rimanenti. Questa tecnica è oggetto di severe critiche e pone complessi quesiti sia in campo etico che in campo legale.
Per evitare di dover sottoporre le donne a ripetute stimolazioni ovariche (sulle cui conseguenze si nutrono alcuni timori) si preferisce, in molti laboratori, produrre un numero di embrioni in eccesso rispetto al bisogno, per poi congelare gli embrioni sovrannumerari, da utilizzare in seguito, anche a distanza di anni (la sopravvivenza degli embrioni congelati è ancora buona dopo 5 anni e non si conoscono i limiti della loro vitalità biologica al freddo; fig. 3).
Complicazioni delle fecondazioni assistite. - Le terapie di stimolo sull'ovaia, anche se eseguite con tutte le cautele necessarie, possono stimolare in eccesso le ovaie, fino a determinare la comparsa di una vera e propria sindrome.
La sindrome da iperstimolazione ovarica è, in effetti, una temuta complicazione non solo delle f. assistite, ma di tutte le stimolazioni ovariche. Mentre le forme di iperstimolazione più lievi rappresentano solo un segnale di rischio e non richiedono molto di più di un periodo di osservazione e qualche controllo ecografico, le più severe possono rappresentare un rischio per la salute e - in casi fortunatamente rarissimi - per la vita stessa della donna. La sindrome si manifesta clinicamente solo qualche giorno dopo il termine del trattamento, ma la sua comparsa può essere sospettata già durante la stimolazione ovarica per la peculiarità della risposta ormonale e follicolare agli stimoli. Nei casi più gravi si possono osservare grandi versamenti di liquido nel peritoneo e negli spazi pleurici, diminuzione della diuresi, ispessimento del sangue, alterazioni elettrolitiche e coagulative. La terapia è sintomatica ed è basata soprattutto sul ripristino della funzione renale e sul controllo dei disturbi dell'equilibrio elettrolitico e della coagulazione. La durata complessiva dei disturbi - talora superiore ai trenta giorni - può subire un ulteriore prolungamento per l'instaurarsi di una gravidanza, così che può essere opportuno, quando la sindrome sia prevedibile, non trasferire gli embrioni prodotti, ma congelarli per un trasferimento in un successivo ciclo naturale.
Altre complicazioni possibili delle f. assistite sono, oltre alle gravidanze multiple, le gravidanze extrauterine. È probabile, però, che la complicazione più temibile sia da identificare nella delusione, visto che la percentuale di successi per ciclo di trattamento non supera il 30÷35% nelle donne più giovani e scende sotto il 10% nelle donne quarantenni, con risultati assolutamente negativi dopo i 43 anni.
I problemi etici. - La produzione di embrioni sovrannumerari e il congelamento degli embrioni ha posto un problema bioetico, che è quello relativo allo statuto dell'embrione. Per molti (e in particolare per la Chiesa cattolica) la vita personale ha inizio con la f. e lo 'spreco' degli embrioni, sia quello legato alla tecnica per sé, sia quello dovuto alla produzione di embrioni sovrannumerari, merita una severa condanna morale. Altri (biologi, filosofi ed esperti di bioetica, anche appartenenti al mondo cattolico) ritengono che esista una fase 'pre-embrionale' identificabile nella fase pre-somatica e pre-individuale dell'embrione, alla quale non possono essere riconosciuti i diritti e le prerogative della persona. Su questo tema, così complesso e delicato, hanno del resto legiferato in modo difforme molti paesi europei (Spagna e Inghilterra, per es., a favore del concetto di pre-embrione; Germania e Austria, contro). Per una più ampia trattazione a tal riguardo, v. bioetica, in questa Appendice.
Attualmente, soprattutto in molti ospedali cattolici e, per legge, in alcuni paesi, viene offerta agli utenti la cosiddetta tecnica del caso semplice, che prevede la f. di un numero di ovociti molto limitato, in modo che non possa essere realizzata la produzione di embrioni sovrannumerari; chi accetta questa tecnica, deve essere consapevole di accettare contemporaneamente una diminuzione delle probabilità di successo, dovuta al fatto che la percentuale di f. non è mai pari al 100%.
Il congelamento degli ovociti. - Per cercare di ridurre il numero di embrioni congelati, il cui accumulo nelle teche degli ospedali e delle cliniche rappresenta un forte motivo di turbamento per molti, è stato sperimentato con successo il congelamento degli ovociti (E. Porcu, 1996), che possono essere conservati anche per lunghi periodi di tempo e utilizzati per le f. in vitro in caso di insuccesso del primo tentativo eseguito con ovociti 'freschi'. Il congelamento degli ovociti può anche rappresentare un metodo per conservare la propria fertilità qualora fossero necessarie terapie sterilizzanti. Si può quindi prevedere la possibilità di organizzare, per l'avvenire, vere e proprie banche di ovociti, a somiglianza di quanto viene già fatto per gli spermatozoi. La possibilità di portare a maturazione in vitro ovociti immaturi ha anche dischiuso una nuova possibilità, per ora soltanto esplorata, che riguarda il congelamento di frammenti d'ovaia (o di ovaia intera) dai cui follicoli estrarre gli ovociti necessari per una f. assistita.
La microiniezione: la ICSI. - Nei primi anni Novanta è stata messa a punto una nuova tecnica di f. in vitro che prevede l'iniezione di singoli spermatozoi nell'ooplasma degli ovociti, mediante un sistema microiniettivo. La tecnica ICSI (Intra Cytoplasmic Sperm Injection), che consente di ottenere gravidanze a partire da campioni di seme estremamente poveri (bastano poche decine di spermatozoi mobili per avere successo), ha ridotto in modo straordinario il numero degli uomini sterili, anche perché è oggi possibile prelevare direttamente, per aspirazione, spermatozoi dall'epididimo e dal testicolo di uomini azoospermici (cioè con eiaculato privo di spermatozoi o per assenza dei dotti deferenti che conducano il seme all'esterno, o per gravi forme di arresto della maturazione delle cellule germinali). Sono state addirittura ottenute gravidanze utilizzando, per l'iniezione intracitoplasmatica, spermatidi, cioè i precursori degli spermatozoi (J. Tesarik, 1996). Anche se i dati relativi alle caratteristiche dei bambini nati con queste tecniche (si contano già molte migliaia di bambini nati con l'ICSI tradizionale, mentre i bambini nati per microiniezione di spermatidi sono pochissimi) sono tranquillizzanti, esiste qualche timore sia per quanto riguarda un possibile incremento di anomalie genetiche relative ai cromosomi sessuali, sia per quanto concerne la possibilità di dover verificare, tardivamente, la comparsa di anomalie dovute a difetti genetici correlati con l'incompleta maturazione dei gameti.
La GIFT. Una tecnica più semplice (dal punto di vista del laboratorio), ma più invasiva della FIVET (dal momento che in genere comporta una laparoscopia), è la GIFT (Gamete Intra Falloppian Transfer), proposta da R. Asch nel 1984 e utilizzata con successo in una serie di condizioni di sterilità di coppia (sterilità da cause ignote; diminuzione della fertilità maschile; alterazioni della parte distale delle tube). Questa tecnica è del tutto simile alla FIVET per quanto riguarda la stimolazione ovarica e il prelievo degli ovociti; ottenuti i gameti, questi (spermatozoi e ovociti) vengono inseriti in un sottile catetere e poi iniettati all'interno di una o di entrambe le tube (in genere per via laparoscopica, ma anche attraverso l'utilizzo di strumenti che consentono di raggiungere le tube attraverso l'utero, come il falloppioscopio o l'isteroscopio.
Con alcune cautele, relative soprattutto al modo con cui viene raccolto il seme e alla mancanza di contatti tra i gameti prima del loro inserimento nelle tube, la tecnica può essere eseguita con il placet della Chiesa cattolica, che la considera un semplice aiuto alla fertilità spontanea.
Le indagini genetiche pre-impianto. - Le tecniche di f. assistita consentono di eseguire nell'embrione, prima dell'impianto, indagini genetiche rivolte a identificare alcune malattie non compatibili o poco compatibili con una normale qualità di vita, in modo da poter evitare il trasferimento nell'utero della madre di embrioni malati (A.H. Handyside, 1990). La tecnica prevede il prelievo di una o più cellule embrionali o dei soli globuli polari e permette di anticipare indagini generalmente eseguite a gravidanza avvenuta con l'amniocentesi o il prelievo dei villi coriali.
Mediante due tecniche di biologia molecolare - la PCR (Polymerase Chain Reaction) e l'ibridazione in situ con fluorescenza o FISH (Fluorescent In Situ Hybridization) - può essere eseguita la determinazione del sesso e possono essere diagnosticate specifiche mutazioni a carico di un singolo gene.
La diagnosi pre-impianto non ha, per ora, altre soluzioni possibili se non quella del sacrificio di un embrione: in tempi non molto lontani sarà invece possibile la terapia genica del prodotto del concepimento, mediante, per es., l'introduzione di un gene normale in grado di sostituire quello alterato o mancante.
Le tecniche di f. assistita, con la diffusione della FIVET, hanno anche reso possibili soluzioni (non tutte accettate e non tutte accettabili) di problemi complessi non sempre collegati con il concetto clinico di sterilità.
La donazione di ovociti. - È possibile in questi ultimi tempi, con la donazione di ovociti, consentire la maternità a donne che non avrebbero potuto avere figli (essendo intervenuta la menopausa) o che non avrebbero voluto averne (per timore di trasmettere loro malattie genetiche). La donazione di ovociti, che riequilibra la condizione femminile rispetto alla possibilità di donazione di spermatozoi, ha però riflessi del tutto particolari in campo etico e sociale, poiché consente la maternità a donne non più giovani, per le quali si debbono considerare problemi di salute (dopo i 50 anni la gravidanza non può essere considerata comunque fisiologica) e problemi relativi alla capacità di rapportarsi in modo adeguato al figlio, capacità non sempre presente nelle persone più anziane.
L'accesso ai trattamenti. - Su questo tema esiste un vivace dibattito bioetico che riguarda anche, in termini più ampi, il diritto di accesso alle f. assistite da parte di alcune categorie di persone (le donne sole, le coppie non sposate, le coppie omosessuali). La discussione riguarda soprattutto l'alternativa tra 'principio famiglia' e 'libertà individuale', e gli elementi in causa sono soprattutto il diritto alla procreazione, il diritto di eguaglianza tra gli individui e, ancora, i diritti del nascituro.
Su tutti questi temi, le legislazioni attualmente esistenti in vari paesi propongono modelli decisionali tra loro differenti, alcuni dei quali consentono la f. artificiale solo se è possibile presumere che il bambino cresca in un ambiente favorevole, mentre altri ritengono di dover privilegiare l'accesso ai trattamenti solo per coloro che accettino formalmente di assumersi le responsabilità della procreazione.
La donazione di embrioni. La maternità surrogata. - La possibilità che si eseguano anche doni di embrioni (estesi, per es., agli embrioni congelati che vengono abbandonati dalle coppie) ha posto sul tappeto anche l'opportunità di costruire cammini paralleli per le coppie che desiderano adottare un bambino e quelle che aspirano a questa sorta di 'adozione prenatale'. Oggetto di attenzioni prevalentemente critiche è poi la maternità surrogata, con la quale una donna fertile ospita nel proprio utero l'embrione di una coppia che, per varie ragioni (assenza dell'utero; presenza di malattie incompatibili con la gravidanza), non è in grado, con le proprie forze, di avere un figlio.
L'impegno della madre surrogata, di condurre a termine la gravidanza nel migliore dei modi per poi consegnare il bambino ai genitori genetici, può basarsi su un atto di solidarietà (maternità surrogata oblativa) o rappresentare più semplicemente la conclusione di un accordo contrattuale. Quest'ultimo tipo di maternità ritenuto illegittimo e non consentito nella maggior parte dei paesi che hanno legiferato su questi temi, trova applicazione soltanto negli Stati Uniti.
La situazione italiana. - In Italia, le tecniche di f. assistita trovano ampia diffusione in alcune strutture pubbliche e in molte istituzioni private. L'assenza di una legge specifica ha lasciato ampi spazi a comportamenti non sempre irreprensibili che hanno più volte suscitato scandali e polemiche. Al momento, le uniche indicazioni per comportamenti medici corretti vengono dalle norme deontologiche dell'Ordine dei medici, che vietano l'ovodonazione in età post-menopausale e l'accesso ai trattamenti alle donne sole e alle coppie omosessuali. La discussione preliminare trova accordo quasi unanime per quanto riguarda la necessità di garantire i diritti dei bambini nati, quali che siano le modalità che ne hanno consentito la nascita. Esiste inoltre il timore di uno sconfinamento delle norme imposte alla fertilità 'artificiale', che potrebbero contagiare l'attiguo territorio della fertilità 'naturale', limitandone i principi di libertà. In data 26 maggio 1999 la Camera dei deputati ha approvato un progetto di legge in materia di procreazione medicalmente assistita. Il progetto di legge è stato trasmesso al Senato per la definitiva approvazione, ma è emerso un rilevante dissenso, il quale investe sia i principi generali che lo informano, sia i contenuti specifici delle disposizioni che sono state adottate. Nel testo approvato dalla Camera è stabilito il divieto della f. eterologa assistita con gameti di donatori esterni alla coppia, coniugata o di fatto, ed è riconosciuta l'adottabilità dei soli embrioni congelati già esistenti (il congelamento sarà vietato a decorrere dalla data di entrata in vigore della legge).
Possibili sviluppi delle tecniche. - I progressi delle conoscenze scientifiche nel campo della fisiologia della riproduzione umana sono molto rapidi e aprono continuamente nuovi scenari. Sono allo studio tecniche di laboratorio che dovrebbero consentire la maturazione in vitro degli spermatozoi a partire da elementi cellulari immaturi (spermatogoni e spermatociti) e, analogamente, si è molto progredito per quanto concerne la maturazione extra-corporea di ovociti immaturi. Dovrebbe essere presto possibile il congelamento di frammenti ovarici (o di ovaie intere) da utilizzare per il recupero di ovociti a distanza di anni dal momento del prelievo. Anche se la clonazione (che consiste nella possibilità di riprodurre un individuo utilizzando il nucleo di una sua cellula differenziata inserita nell'ooplasma di un uovo privato del nucleo; v. clonazione, in questa Appendice) sembra raccogliere soltanto critiche per quanto riguarda una sua possibile applicazione in campo umano, sono allo studio tecniche di utilizzazione delle cellule embrionali che consentano la produzione di gemelli identici e che migliorino le probabilità di successo delle f. assistite. Sono state invece ovunque bandite le sperimentazioni relative alla fusione tra genomi di specie diverse, all'ectogenesi e alla formazione di chimere.
bibliografia
P. Singer, Practical ethics, Cambridge-New York 1979 (trad. it. Napoli 1989).
H.T. Engelhardt jr., The foundations of bioetics, New York-London 1986 (trad. it. Manuale di bioetica, Milano 1991).
M. Mengarelli, Produrre la riproduzione. Riflessioni sulle questioni etiche e sui significati sociali delle tecnologie applicate alla riproduzione umana, Palermo 1986.
R. Dulbecco, Ingegneri della vita, Milano 1988.
N.M. Ford, When did I begin?, Cambridge-New York 1988 (trad. it. Milano 1997).
C. Melega et al., Organizzazione di un centro pubblico per la terapia della sterilità, in Medicina della riproduzione. Prospettive terapeutiche per gli anni Novanta, a cura di M. Filicori, C. Flamigni, Bologna 1988.
E. Sgreccia, Manuale di bioetica, Milano 1988.
Bioetica, a cura di A. Di Meo, C. Mancina, Roma-Bari 1989.
E. Cittadini, F. Gattuccio, G.B. La Sala et al., La sterilità umana, Palermo 1990.
H. Yonas, Il principio di responsabilità, Torino 1990.
G. Berlinguer, Questioni di vita: etica, scienza e salute, Torino 1991.
J. Harris, Wonderwoman and superman. The ethics of human biotechnology, Oxford-New York 1992 (trad. it. Milano 1997).
Introduzione alla bioetica, a cura di G. Ferranti, S. Maffettone, J.J. Thomson, Napoli 1992.
M.J. Charlesworth, Bioethics in a liberal society, New York 1993 (trad. it. Roma 1996).
R.M. Dworkin, Life's dominion. An argument about abortion, euthanasia and individual freedom, New York 1993 (trad. it. Milano 1994).
E.E. Philipp, Impact of the fertilization and embriology act (1990) on the practice of reproductive medicine in the United Kingdom, in Fertility and sterility, 1993, 59, pp. 285-87.
Questioni di bioetica, a cura di S. Rodotà, Bari 1993.
Y.P. Toner, G.D. Hogden, The future of assisted technologies, in Assisted reproductive technologies, ed. R.P. Marrs, Boston (Mass.) 1993.
A. Bompiani, Bioetica dalla parte dei deboli, Bologna 1994.
C. Flamigni, I laboratori della felicità. La cura della sterilità fra successi e delusioni, Milano 1994.
Itinerari bioetici, a cura di M. Callari Galli, Scandicci 1994.
M. Cantarelli, E. Cittadini, E. Cefalù et al., Biologia della riproduzione umana, Palermo, 1995.
R.G. Edwards, S.A. Brody, Principles and practice of assisted human reproduction, Philadelphia (Pa.) 1995.
F.D. Ginsburg, R. Rapp, Conceiving the new world order, the global politics of reproduction, Berkeley (Calif.) 1995.
M. Mori, La fecondazione artificiale. Una nuova forma di riproduzione umana, Roma-Bari 1995.
S. Rodotà, Tecnologie e diritti, Bologna 1995.
V. Franco, Etiche possibili. Il paradosso della morale dopo la morte di Dio, Roma 1996.
Th. Rabe, K. Driedrich, B. Reinnebaun, Manual on assisted reproduction, Berlin-New York 1996.
Reproductive endocrinology surgery and technology, ed. E.Y. Adashi, J.A. Rock, Z. Rosenwaks, Philadelphia (Pa.) 1996.
S. Vegetti Finzi, Volere un figlio, Milano 1997.
E. Porcu, C. Flamigni, Human oocytes: from physiology to IVF, Bologna 1998.
Frontiere della vita, vol. 4°, 3ª parte: Bioetica, a cura di L. De Carli, S. Rodotà, Istituto della Enciclopedia Italiana, Roma 1999.
E. Lecaldano, Bioetica. Le scelte morali, Roma-Bari 1999.