NGF, fattore
NGF (sigla dell’ingl. Nerve Growth Factor), fattore
Polipeptide che svolge un’azione trofica, tropica e differenziativa su cellule neuronali e non neuronali, ma correlate al sistema nervoso, come le cellule endocrine e immunitarie. È il capostipite della famiglia delle neurotrofine (➔). L’NGF è prodotto nell’ippocampo, nella corteccia cerebrale e nell’ipotalamo come una pre-proteina, il proNGF, che è successivamente processata da alcuni enzimi (convertasi) per dare la forma matura di NGF, che viene secreta all’esterno della cellula.
Scoperta
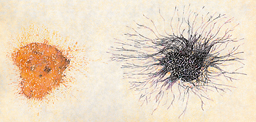
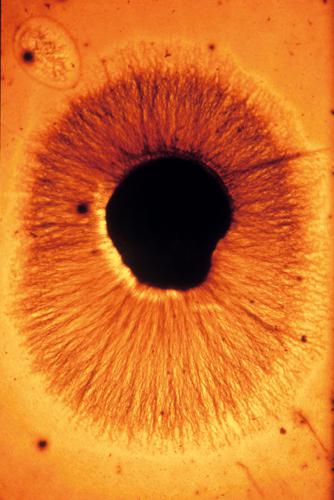
L’NGF fu scoperto nel 1948 da R. Levi Montalcini che per tale scoperta fu insignita del premio Nobel per la medicina o la fisiologia nel 1986. La scienziata italiana lo identificò come una sostanza capace di indurre una straordinaria crescita delle fibre nervose intorno a un ganglio nervoso (un piccolo ammasso di cellule nervose al di fuori del sistema nervoso centrale): un fenomeno definito come effetto dell’alone fibrillare (halo effect). Oggi l’NGF è conosciuto come un fattore che svolge un ruolo cruciale nei processi di sopravvivenza e di differenziamento durante le fasi di sviluppo pre- e postnatale e in molteplici aspetti della fisiologia dell’adulto.
Funzione
Le azioni sulle cellule bersaglio avvengono grazie al legame dell’NGF maturo a due tipi di recettori di membrana: un recettore glicoproteico transmembrana, p75NTR, che lega le neurotrofine con eguale affinità, e un recettore ad attività tirosinchinasica, TrkA, che riconosce selettivamente l’NGF. A seguito del legame con il recettore, l’NGF è trasportato lungo gli assoni, prevalentemente attraverso il classico trasporto retrogrado, ossia che procede dalle terminazioni nervose verso il corpo cellulare. Alcuni studi hanno evidenziato anche la sua capacità di raggiungere le terminazioni nervose attraverso il trasposto anterogrado rapido (dal corpo cellulare, dove viene sintetizzato, alla sinapsi, a livello della quale viene secreto) con il risultato di accelerarne gli effetti di segnalazione. In condizioni fisiologiche il legame di NGF maturo con i due recettori promuove la sopravvivenza cellulare, poiché TrkA media il segnale di sopravvivenza e sopprime il segnale che induce la morte cellulare (apoptosi) proveniente da p75. Negli stati patologici, il segnale di sopravvivenza di NGF è alterato, o per un aumento di concentrazione di proNG, che si lega e attiva preferenzialmente p75, o per la sovraespressione di p75 stesso. L’effetto risultante è il predominio del segnale pro-apoptotico di p75. Diversi studi hanno evidenziato le potenziali proprietà terapeutiche dell’NGF nei meccanismi di plasticità e di riparo del tessuto nervoso in patologie neurodegenerative (morbo di Alzheimer, lesioni cerebrali o del midollo spinale), malattie autoimmuni (sclerosi multipla), patologie oftalmiche e patologie cutanee.